Neue therapeutische Perspektiven für die traditionelle Medizin: ABPP-Technologie enthüllt Berberins neuartiges entzündungshemmendes Ziel EIF2AK2
Die traditionelle Medizin wird durch neue pharmakologische Anwendungen wiederbelebt, da fortschrittliche Techniken wie das aktivitätsbasierte Proteinprofiling (ABPP) Licht auf bisher unbekannte therapeutische Mechanismen werfen. In diesem Zusammenhang hat die ABPP-Technologie kürzlich ein neuartiges entzündungshemmendes Ziel von Berberin entdeckt, einer Verbindung, die aus traditionellen chinesischen Heilpflanzen gewonnen wird und in China allgemein als Coptisin oder Huanglian bekannt ist. Die Entdeckung unterstreicht, dass EIF2AK2 eine Schlüsselrolle bei der entzündungshemmenden Wirkung von Berberin spielt und eröffnet neue Möglichkeiten für seinen Einsatz bei der Behandlung entzündungsbedingter Erkrankungen. Dieser Durchbruch unterstreicht das Potenzial für die Umnutzung und Optimierung traditioneller Arzneimittel durch moderne wissenschaftliche Methoden.

Berberin, ein traditionelles Alkaloid mit weitreichenden pharmakologischen Wirkungen, darunter Entzündungshemmung, Hypoglykämie und Herz-Kreislauf-Schutz, hat große Aufmerksamkeit erregt. Die genauen molekularen Mechanismen, insbesondere bei der Unterdrückung von Entzündungen, sind jedoch weiterhin unklar.
Diese Studie schließt diese Wissenslücke mithilfe der ABPP-Technologie, um EIF2AK2 als kritisches Ziel zu identifizieren, an dem Berberin aufgrund seiner entzündungshemmenden Wirkung beteiligt ist. Die Ergebnisse vertiefen unser Verständnis des Mechanismus von Berberin und liefern eine wissenschaftliche Grundlage für die Neupositionierung von Berberin und die Entwicklung neuer, auf EIF2AK2 ausgerichteter entzündungshemmender Medikamente.
Das Team nutzte fortschrittliche chemoproteomische Methoden, um die Wechselwirkungen von Berberin mit intrazellulären Proteinen systematisch zu untersuchen und seine spezifische Bindung an EIF2AK2 und die Modulation seiner enzymatischen Aktivität zu bestätigen. Dies beeinflusst die Entzündungsreaktionswege und hemmt wirksam das Fortschreiten der Entzündung. Dieser bedeutende Durchbruch bietet Einblicke in den entzündungshemmenden Mechanismus von Berberin und unterstützt die Entwicklung neuartiger Therapien gegen EIF2AK2.
ChomiX bietet hochmoderne Dienste wie ABPP und CETSA, um Forscher bei der Erforschung von Arzneimittelmechanismen und der Beschleunigung neuer Arzneimittelentwicklungsbemühungen zu unterstützen.
Forschungsroute
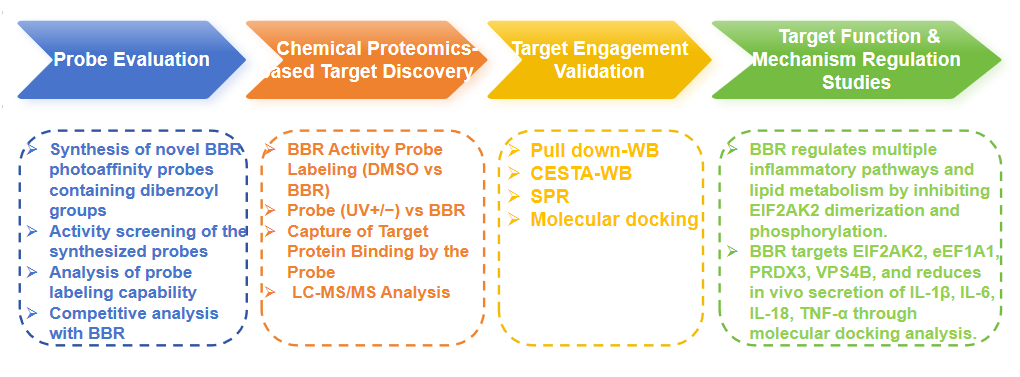
Experimenteller Prozess
1. Sonde 11b wurde als funktionelles Werkzeug in der Proteomikforschung eingesetzt.
Die Autoren synthetisierten und testeten neuartige BBR-Photoaffinitätssonden mit Dibenzoylgruppen in LPS + Nigericin-aktivierten THP-1-Makrophagen. Unter diesen zeigten die Verbindungen 7a und 11b zeit- und dosisabhängige Hemmwirkungen auf die IL-1β-Expression und zeigten eine verbesserte Wirksamkeit im Vergleich zur Ausgangsverbindung BBR. Mithilfe der Analyse des aktivitätsbasierten Proteinprofils (ABPP) und des Fluoreszenzscans wurde nachgewiesen, dass sowohl 7a als auch 11b effektiv an ihre Zielproteine binden und eine kompetitive Hemmung zeigen, was auf einen Wirkmechanismus hinweist, der dem von BBR ähnelt. Basierend auf der Beobachtung, dass Verbindung 11b deutliche Veränderungen der Fluoreszenzintensität im Konzentrationsbereich von 2,5 % bis 25 % aufwies, insbesondere bei einer Konzentration von 20 Millimolar, wo die Variation des Fluoreszenzsignals am deutlichsten war, wurde sie als funktionelle Sonde für Proteomikstudien ausgewählt . Diese Auswahl beruhte auf seiner überlegenen Reaktionsfähigkeit, die es für die Aufklärung von Proteininteraktionen in einem proteomischen Umfeld geeignet macht.
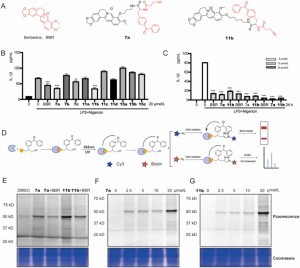
Abbildung 1: Screening und Bewertung von BBR-Sonden.
2. Die neuartige Sonde 11b hat 44 entzündungsbedingte Zielproteine von BBR in THP-1-Zellen identifiziert und EIF2AK2, eEF1A1, PRDX3 und VPS4B als direkte Ziele mit spezifischen Wechselwirkungen mit BBR identifiziert.
In einer Reihe von Experimenten setzten die Autoren die neuartige Sonde 11b erfolgreich ein, um potenzielle Zielproteine in THP-1-Zellen zu markieren und zu reinigen. Anschließend identifizierten sie mithilfe einer LC-MS/MS-Analyse 44 entzündungsassoziierte Proteine im Molekulargewichtsbereich von 20 bis 80 kDa, von denen sechs möglicherweise eine entscheidende Rolle bei der entzündungshemmenden Wirkung von BBR spielten. In weiteren Untersuchungen wurde bestätigt, dass EIF2AK2, eEF1A1, PRDX3 und VPS4B direkte Ziele von BBR sind und unter hohen Konzentrationen der BBR-Behandlung kompetitive Hemmwirkungen zeigen. Dieser Befund offenbarte die wahrscheinliche Existenz spezifischer Wechselwirkungen zwischen diesen Proteinen und BBR und lieferte so neue Einblicke in ihre Interaktion mit dem Medikament während seiner entzündungshemmenden Prozesse.
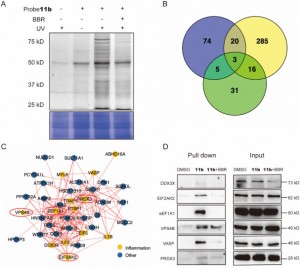
Abbildung 2: Erfassung und Funktionsanalyse von Zielproteinen.
3. Die strukturbiologische Forschung erläutert, wie BBR die EIF2AK2-Dimerisierung moduliert, um seine entzündungshemmende Wirkung durch kritische Ionenwechselwirkungen und Kation-Pi-Bindung auszuüben.
Die Autoren verwendeten CETSA-, SPR- und molekulare Docking-Techniken, um die Wechselwirkungen zwischen BBR und vier Proteinen – EIF2AK2, eEF1A1, PRDX3 und VPS4B – in HEK-293-Zellen zu validieren. Die Ergebnisse zeigten, dass BBR die thermische Stabilität dieser vier Proteine erhöhte, wobei die stärkste Affinität für EIF2AK2 beobachtet wurde. Weitere Untersuchungen ergaben, dass die Bindung von BBR an EIF2AK2 hauptsächlich auf Ionenpaaren beruht, an denen D316 und E367 in Hohlraum II beteiligt sind, sowie auf Kation-Pi-Wechselwirkungen mit K291. Diese Bindungsstelle ist an der EIF2AK2-Dimerisierung beteiligt, was darauf hindeutet, dass BBR seine entzündungshemmende Wirkung möglicherweise durch Modulation der EIF2AK2-Dimerisierung entfaltet.
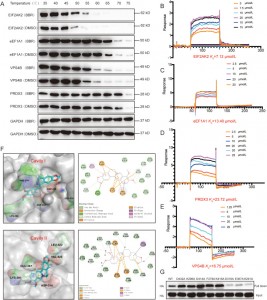
Abbildung 3: Affinitätsstudien zwischen BBR und seinen potenziellen Zielen.
4. Die Rolle von BBR bei Entzündungen und Lipidstoffwechselwegen wird aufgezeigt, da es die EIF2AK2-Dimerisierung und -Phosphorylierung hemmt, wodurch eine zentrale Funktion bei der Regulierung des NLRP3-Inflammasoms und der NF-kB p65/JNK/SIRT1-Signalisierung nachgewiesen wird.
Immunpräzipitationsexperimente bestätigten, dass BBR die Dimerisierung von EIF2AK2 hemmt und sowohl die Autophosphorylierung von EIF2AK2 als auch die Phosphorylierung seines Substrats eIF2a beeinflusst. Dies zeigt, dass BBR das NLRP3-Inflammasom, NF-kB p65, die JNK-Signalwege und die SIRT1-Expression reguliert und eine entscheidende Rolle bei zellulären Entzündungsreaktionen spielt. entzündungshemmende Mechanismen des Gehirns (z. B. bei der Alzheimer-Krankheit) und Fett Säureinduzierter endoplasmatischer Retikulumstress. Darüber hinaus veränderte die Stummschaltung oder Überexpression von EIF2AK2 die regulatorischen Wirkungen von BBR auf p-JNK und SIRT1 erheblich, was weiter untermauert, dass BBR durch Bindung an EIF2AK2 entzündungsbedingte Lipidstoffwechselstörungen reguliert.
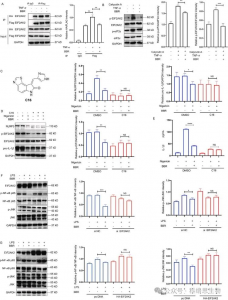
Abbildung 2 Zielproteinerfassung und Funktionsanalyse.
5. Indem BBR auf EIF2AK2, eEF1A1, PRDX3 und VPS4B abzielt, passt es mehrere Entzündungswege an, wobei EIF2AK2 unter diesen Zielen eine dominierende regulatorische Rolle spielt.
Um diese Wechselwirkung weiter zu untersuchen, erstellten die Autoren Überexpressions- und Knockdown-Modelle der vier Proteine und zeigten, dass BBR die Entzündungswege JNK, NF-kB, MAPK und AKT selektiv moduliert, wobei EIF2AK2 eine dominierende Rolle spielt, was in In-vivo-Experimenten validiert wurde .
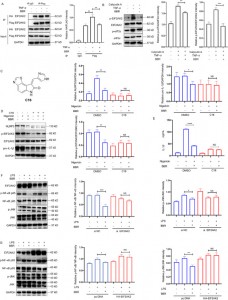
Abbildung 5: Funktionsstudien der BBR-Zielproteine
6. Durch spezifisches Targeting von EIF2AK2 reguliert BBR die In-vivo-Sekretion von IL-1β, IL-6, IL-18 und TNF-α herunter; Durch den Abbau des EIF2AK2-Gens werden dessen entzündungshemmende Wirksamkeit und leberschützende Wirkung verringert.
Anschließend untersuchten sie, ob BBR die Freisetzung von IL-1β, IL-6, IL-18 und TNF-α beeinflusst, indem es in vivo auf EIF2AK2 abzielt. Zu diesem Zweck erstellten sie ein EIF2AK2-Gen-Knockout-Mausmodell durch intravenöse Injektion eines Adeno-assoziierten Virus (AAV), das shEIF2AK2 trägt. Wildtyp- und EIF2AK2-Knockout-Mäusen wurde BBR (3 mg/kg) intraperitoneal verabreicht, gefolgt von einer LPS-Injektion. Während BBR die Spiegel von IL-1β, IL-6, IL-18 und TNF-α in der Kontrollgruppe signifikant reduzierte, war dieser Effekt in der EIF2AK2-Knockout-Gruppe abgeschwächt. Die histologische Untersuchung mittels H&E-Färbung von Lebergewebe zeigte, dass die verbessernde Wirkung von BBR auf die Infiltration von Leberentzündungen bei EIF2AK2-Knockout-Mäusen abgeschwächt war. Diese Ergebnisse legen nahe, dass BBR möglicherweise die Sekretion von IL-1β, IL-6, IL-18 und TNF-α herunterreguliert, indem es auf EIF2AK2 abzielt, und eine gute Sicherheit aufweist.
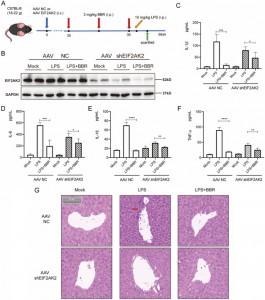
Abbildung 6: Funktionsüberprüfungen von EIF2AK2 in vivo.
Diese Studie demonstriert umfassend die leistungsstarken Vorteile der ABPP-Technologie bei der Aufklärung der komplexen Mechanismen bioaktiver Moleküle wie Berberin und treibt den Fortschritt der modernen Forschung zu traditionellen Arzneimitteln voran. Durch die Entdeckung neuer Angriffspunkte und Wirkmechanismen für das alte Medikament Berberin bereichert es nicht nur unser Verständnis der biologischen Funktionen traditioneller Arzneimittel, sondern eröffnet auch neue Perspektiven und Möglichkeiten für die Behandlung entzündungsbedingter Erkrankungen. Dieses Ergebnis deutet darauf hin, dass mit der Unterstützung moderner wissenschaftlicher Techniken wie ABPP traditionellere Arzneimittel durch die Identifizierung ihrer spezifischen Ziele und Mechanismen einem neuen Verwendungszweck zugeführt werden und so einen erheblichen Beitrag zu den Bemühungen um die menschliche Gesundheit leisten werden.

