[Avance de puntuación alta] Avance en la regulación antiinflamatoria de SLC15A4 con el nuevo inhibidor AJ 2-30: un enfoque de proteómica química (IF 14.8)
Este artículo emplea proteómica química para diseñar y seleccionar una variedad de nuevos inhibidores dirigidos a SLC15A4, una proteína transmembrana inflamatoria crucial altamente expresada en células presentadoras de antígenos. La selección inicial de inhibidores potenciales utilizó la estrategia de biblioteca de sondas de fragmentos completamente funcionalizados (FFF), identificando a FFF-21 como un potente inhibidor de la producción de IFN-α entre numerosas sondas. La optimización estructural posterior condujo al desarrollo del compuesto AJ 2-30, que no solo demostró una inhibición sobresaliente sino que también confirmó a SLC15A4 como su objetivo principal después de la modificación de la fotoentrecruzamiento. Investigaciones adicionales revelaron que AJ 2-30 ejerció potentes efectos antiinflamatorios al reducir la estabilidad de SLC15A4, inducir su degradación a través de la vía lisosomal e inhibir eficazmente la activación de TLR 7-9 y NOD. Este estudio no solo es pionero con éxito en los inhibidores de SLC15A4 con una importante actividad antiinflamatoria, sino que también allana el camino para el desarrollo de nuevos fármacos antiinflamatorios.

Ruta de investigación
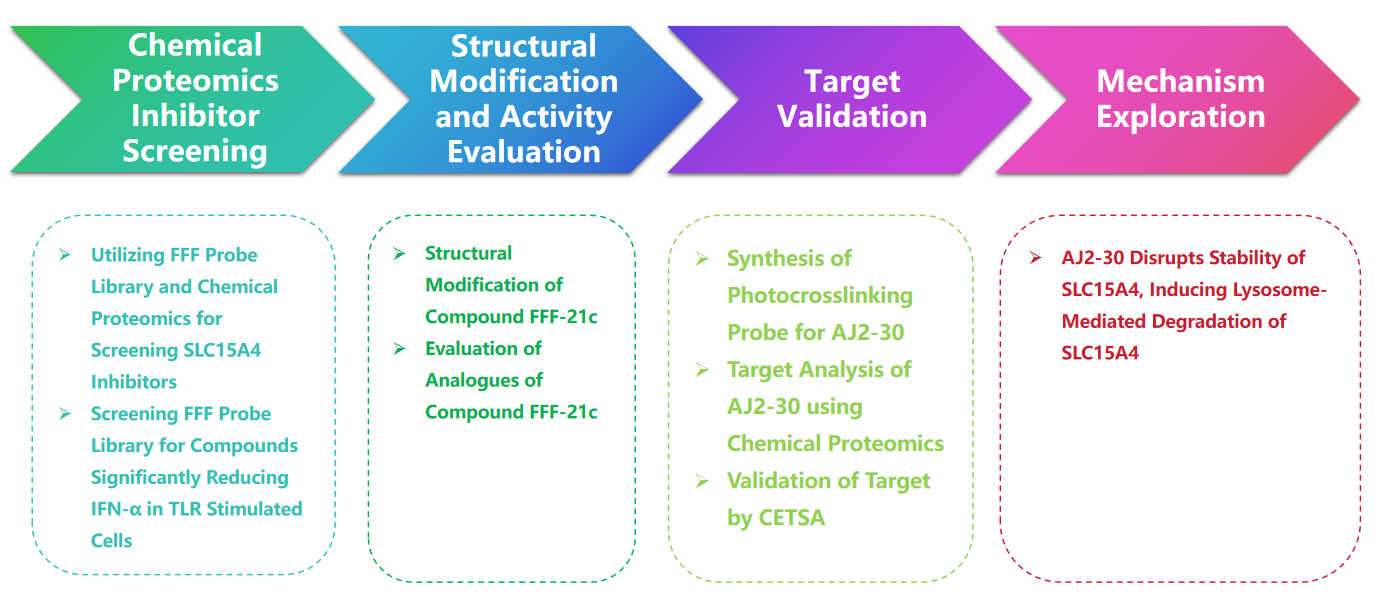
Proceso experimental
1. Estrategia de biblioteca de sondas de fragmentos completamente funcionalizados (FFF) para detectar inhibidores de SLC15A4.
Los autores iniciaron su estudio seleccionando inhibidores de SLC15A4 utilizando una biblioteca de sondas de fragmentos completamente funcionalizados (FFF). Este FFF consta de dos componentes: un grupo de reconocimiento molecular que contiene fragmentos de tabletas diseñados para apuntar a SLC15A4, y otro grupo enriquecido fotoentrecruzado que presenta grupos dobles de acrimidina y alquino para visualizar SLC15A4. Empleando un flujo de trabajo de proteómica química, los autores confirmaron la unión de esta biblioteca de sondas FFF a SLC15A4 en células y evaluaron si la sonda FFF podría atenuar los niveles de IFN-α en células estimuladas con TLR 9. Los resultados demostraron que entre todas las sondas FFF que se unen a SLC15A4, FFF-21 exhibió la mayor capacidad para inhibir los niveles de IFN-α, y su análogo sin marcador, FFF-21c, también mostró efectos inhibidores similares.
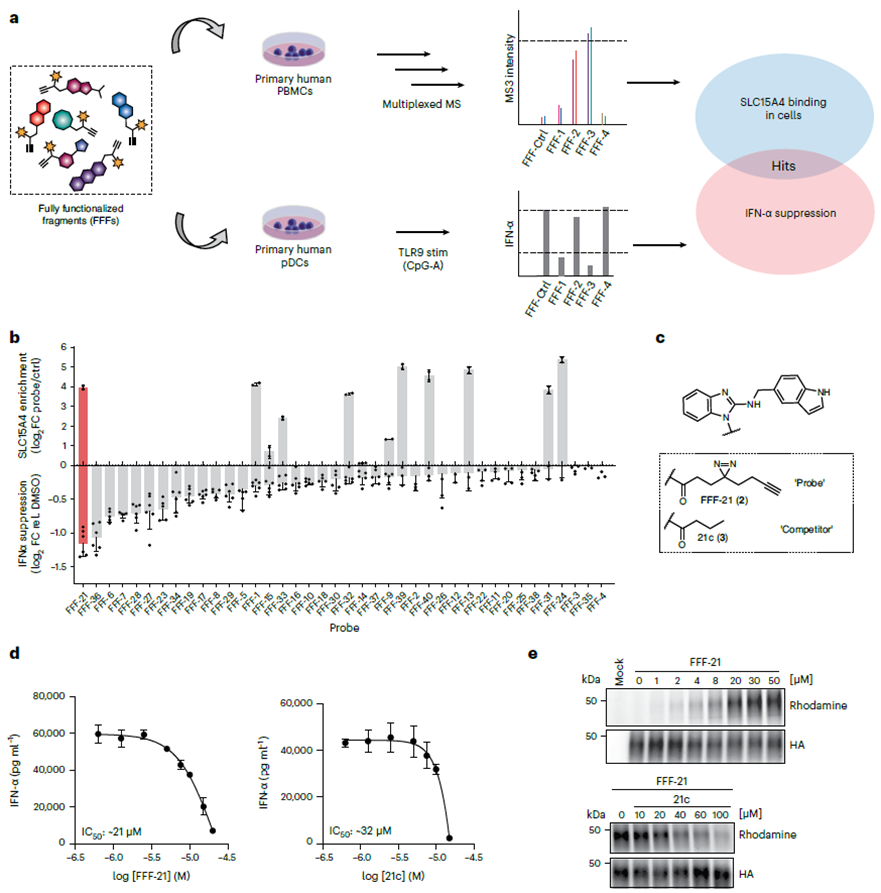
2. Modificación por fotoentrecruzamiento de los inhibidores de SLC15A4.
Tras la selección inicial del compuesto FFF-21c, los autores procedieron a optimizar su estructura. Mediante la síntesis de varios análogos de FFF-21c, identificaron al AJ 2-30 como el inhibidor más potente. Empleando técnicas de fotoentrecruzamiento, confirmaron su interacción con el objetivo. Posteriormente, utilizando tanto el método de etiquetado directo como el método de competencia indirecta de ABPP, junto con el análisis de desplazamiento térmico celular (CETSA), los autores establecieron definitivamente a SLC15A4 como el objetivo principal de AJ 2-30.
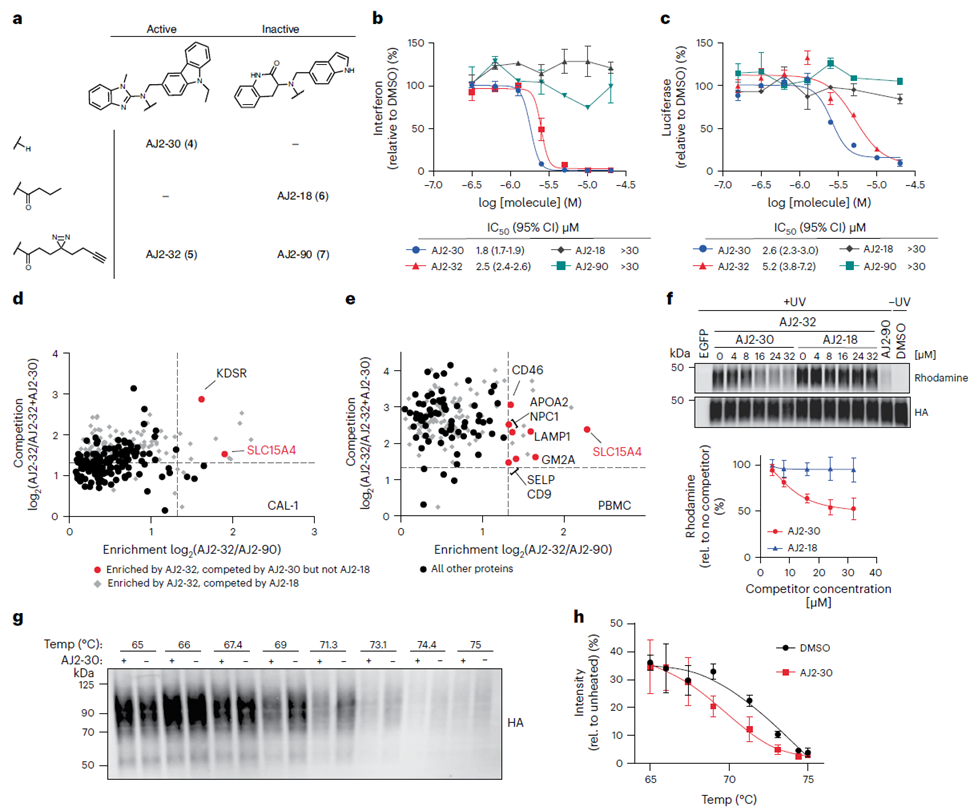
3. El mecanismo antiinflamatorio revela que AJ 2-30 altera la estabilidad de SLC15A4.
Tras la confirmación de la unión de AJ 2-30 a SLC15A4 y su efecto inhibidor, los autores realizaron una serie de experimentos bioquímicos para dilucidar el mecanismo antiinflamatorio de AJ 2-30. Los resultados revelaron que AJ 2-30 induce la degradación mediada por lisosomas de SLC15A4 al desestabilizar la proteína, inhibiendo así la activación de TLR 7-9 y NOD en células inmunes de una manera dependiente de SLC15A4. Esto subraya el potencial de AJ 2-30 en el tratamiento de enfermedades inflamatorias y autoinmunes.
En resumen, este estudio utiliza hábilmente técnicas de proteómica química para identificar AJ 2-30, un potente inhibidor de SLC15A4 con notable actividad antiinflamatoria. Este compuesto demuestra una eficacia significativa en modelos animales al atacar específicamente la estabilidad de SLC15A4 y su papel en la presentación de antígenos y las vías de señalización inflamatoria. Este avance fundamental no sólo mejora nuestra comprensión de los objetivos terapéuticos antiinflamatorios, sino que también sienta una base sólida para el desarrollo futuro de nuevos agentes terapéuticos para una variedad de enfermedades inflamatorias y autoinmunes. Con más investigación y validación clínica, estos nuevos inhibidores de SLC15A4 están preparados para ofrecer opciones de tratamiento más precisas y efectivas para una multitud de pacientes, generando así un profundo impacto en la salud global.

