
Produits
Nouvelles perspectives thérapeutiques pour la médecine traditionnelle : la technologie ABPP dévoile la nouvelle cible anti-inflammatoire de la berbérine EIF2AK2
La médecine traditionnelle est revitalisée avec de nouvelles applications pharmacologiques alors que des techniques avancées telles que le profilage des protéines basé sur l'activité (ABPP) mettent en lumière des mécanismes thérapeutiques jusqu'alors inconnus. Dans ce contexte, la technologie ABPP a récemment révélé une nouvelle cible anti-inflammatoire de la berbérine, un composé extrait de plantes médicinales traditionnelles chinoises et communément appelé Coptisine ou Huanglian en Chine. La découverte met en évidence EIF2AK2 comme un acteur clé dans les effets anti-inflammatoires de la berbérine, ouvrant de nouvelles voies pour son utilisation dans le traitement des maladies liées à l'inflammation. Cette avancée souligne le potentiel de réutilisation et d’optimisation des médecines traditionnelles grâce à des méthodes scientifiques modernes.

La berbérine, un alcaloïde traditionnel aux effets pharmacologiques étendus, notamment anti-inflammatoires, hypoglycémiques et protecteurs cardiovasculaires, a attiré une attention considérable. Cependant, ses mécanismes moléculaires précis, notamment dans la suppression de l’inflammation, restent flous.
Cette étude comble ce manque de connaissances en utilisant la technologie ABPP pour identifier EIF2AK2 comme cible critique engagée par la berbérine pour son action anti-inflammatoire. Les résultats approfondissent notre compréhension du mécanisme de la berbérine et fournissent une base scientifique pour repositionner la berbérine et développer de nouveaux médicaments anti-inflammatoires ciblés sur EIF2AK2.
L'équipe a utilisé des méthodes chimioprotéomiques avancées pour étudier systématiquement les interactions de la berbérine avec les protéines intracellulaires, confirmant ainsi sa liaison spécifique à EIF2AK2 et la modulation de son activité enzymatique. Cela influence les voies de réponse inflammatoire, inhibant efficacement la progression de l’inflammation. Cette avancée significative offre un aperçu du mécanisme anti-inflammatoire de la berbérine et soutient le développement de nouveaux traitements ciblant EIF2AK2.
ChomiX fournit des services de pointe comme ABPP et CETSA pour aider les chercheurs à explorer les mécanismes des médicaments et à accélérer les efforts de développement de nouveaux médicaments.
Itinéraire de recherche
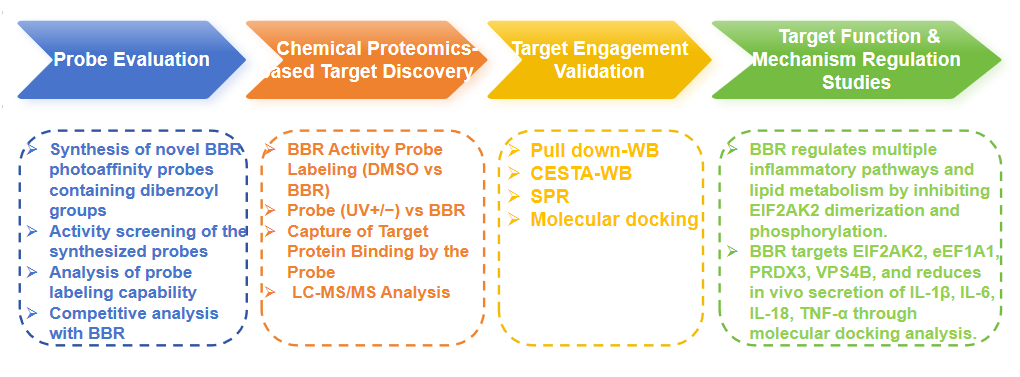
Processus expérimental
1. La sonde 11b a été utilisée comme outil fonctionnel dans la recherche en protéomique.
Les auteurs ont synthétisé et examiné de nouvelles sondes de photoaffinité BBR contenant des groupes dibenzoyle dans les macrophages THP-1 activés par LPS + Nigéricine. Parmi ceux-ci, les composés 7a et 11b ont présenté des effets inhibiteurs dépendants du temps et de la dose sur l'expression de l'IL-1β, démontrant une efficacité accrue par rapport au composé parent BBR. Grâce à l'analyse du profilage des protéines basée sur l'activité (ABPP) et à l'analyse par fluorescence, il a été démontré que 7a et 11b se lient efficacement à leurs protéines cibles et présentent une inhibition compétitive, indiquant ainsi un mécanisme d'action similaire à celui du BBR. Sur la base de l'observation selon laquelle le composé 11b présentait des changements marqués dans l'intensité de la fluorescence dans la plage de concentrations de 2,5 % à 25 %, en particulier à une concentration de 20 millimolaires où la variation du signal de fluorescence était la plus importante, il a été choisi comme sonde fonctionnelle pour les études protéomiques. . Cette sélection repose sur sa réactivité supérieure, ce qui la rend adaptée à l’élucidation des interactions protéiques dans un contexte protéomique.
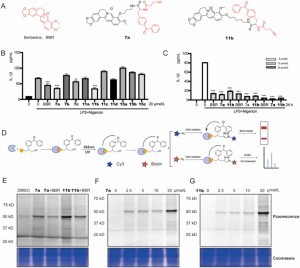
Figure 1 : Criblage et évaluation des sondes BBR.
2. La nouvelle sonde 11b a identifié 44 protéines cibles du BBR liées à l'inflammation dans les cellules THP-1 et a révélé EIF2AK2, eEF1A1, PRDX3 et VPS4B comme cibles directes ayant des interactions spécifiques avec le BBR.
Les auteurs, grâce à une série d'expériences, ont utilisé avec succès la nouvelle sonde 11b pour marquer et purifier les protéines cibles potentielles dans les cellules THP-1. Suite à cela, ils ont utilisé l'analyse LC-MS/MS pour identifier 44 protéines associées à l'inflammation dans la plage de poids moléculaire de 20 à 80 kDa, parmi lesquelles six jouent potentiellement un rôle critique dans les actions anti-inflammatoires du BBR. Au cours d'enquêtes plus approfondies, EIF2AK2, eEF1A1, PRDX3 et VPS4B ont été confirmés comme cibles directes du BBR, présentant des effets d'inhibition compétitifs sous des concentrations élevées de traitement par BBR. Cette découverte a révélé l’existence probable d’interactions spécifiques entre ces protéines et le BBR, élucidant ainsi de nouvelles informations sur leur engagement avec le médicament au cours de ses processus anti-inflammatoires.
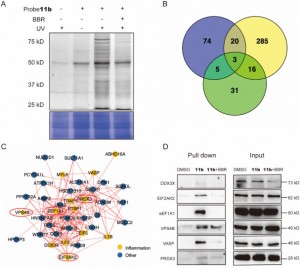
Figure 2 : Capture des protéines cibles et analyse fonctionnelle.
3. La recherche en biologie structurale explique comment BBR module la dimérisation d'EIF2AK2 pour exercer ses effets anti-inflammatoires via des interactions ioniques critiques et la liaison cation-pi.
Les auteurs ont utilisé des techniques CETSA, SPR et d'amarrage moléculaire pour valider les interactions entre BBR et quatre protéines (EIF2AK2, eEF1A1, PRDX3 et VPS4B) dans les cellules HEK-293. Les résultats ont montré que BBR augmentait la stabilité thermique de ces quatre protéines, la plus forte affinité étant observée pour EIF2AK2. Une enquête plus approfondie a révélé que la liaison du BBR à EIF2AK2 repose principalement sur des paires d'ions impliquant D316 et E367 dans la cavité II, ainsi que sur des interactions cation-pi avec K291. Ce site de liaison est impliqué dans la dimérisation d'EIF2AK2, ce qui suggère que le BBR pourrait exercer ses effets anti-inflammatoires en modulant la dimérisation d'EIF2AK2.
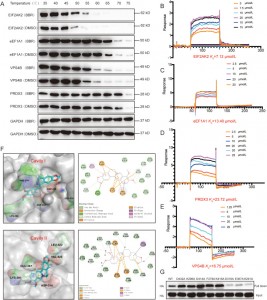
Figure 3 : Études d'affinité entre BBR et ses cibles potentielles.
4. Le rôle du BBR dans les voies de l'inflammation et du métabolisme lipidique est révélé car il inhibe la dimérisation et la phosphorylation d'EIF2AK2, démontrant ainsi une fonction essentielle dans la régulation de l'inflammasome NLRP3, la signalisation NF-kB p65/JNK/SIRT1.
Les expériences d'immunoprécipitation ont confirmé que BBR inhibe la dimérisation de EIF2AK2, affectant à la fois l'autophosphorylation de EIF2AK2 et la phosphorylation de son substrat eIF2a, révélant ainsi que BBR régule l'inflammasome NLRP3, NF-kB p65, les voies de signalisation JNK et l'expression de SIRT1, jouant un rôle crucial dans les réponses inflammatoires cellulaires. mécanismes anti-inflammatoires cérébraux (comme dans la maladie d'Alzheimer) et graisse stress du réticulum endoplasmique induit par l’acide. De plus, la désactivation ou la surexpression d'EIF2AK2 a modifié de manière significative les effets régulateurs de BBR sur p-JNK et SIRT1, confirmant ainsi que BBR agit en se liant à EIF2AK2 pour réguler les troubles métaboliques lipidiques liés à l'inflammation.
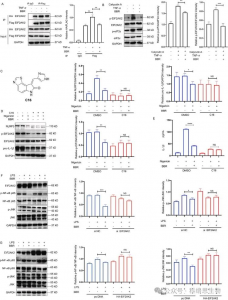
Figure 2 Capture des protéines cibles et analyse fonctionnelle.
5. En ciblant EIF2AK2, eEF1A1, PRDX3 et VPS4B, BBR ajuste plusieurs voies inflammatoires, EIF2AK2 jouant un rôle régulateur dominant parmi ces cibles.
Pour explorer davantage cette interaction, les auteurs ont établi des modèles de surexpression et d'inactivation des quatre protéines, démontrant que BBR module sélectivement les voies inflammatoires JNK, NF-kB, MAPK et AKT, EIF2AK2 jouant un rôle dominant, ce qui a été validé dans des expériences in vivo. .
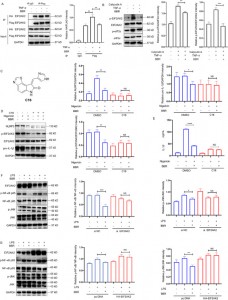
Figure 5 : Etudes fonctionnelles des protéines cibles BBR
6. Grâce au ciblage spécifique d'EIF2AK2, BBR régule négativement la sécrétion in vivo d'IL-1β, d'IL-6, d'IL-18 et de TNF-α ; l'inactivation du gène EIF2AK2 diminue son efficacité anti-inflammatoire et ses actions protectrices du foie.
Ils ont ensuite étudié si le BBR affectait la libération d’IL-1β, d’IL-6, d’IL-18 et de TNF-α en ciblant EIF2AK2 in vivo. Pour ce faire, ils ont créé un modèle de souris knock-out du gène EIF2AK2 en utilisant l’injection intraveineuse d’un virus adéno-associé (AAV) portant shEIF2AK2. Des souris knock-out de type sauvage et EIF2AK2 ont reçu du BBR (3 mg/kg) par voie intrapéritonéale, suivi d'une injection de LPS. Alors que le BBR réduisait de manière significative les niveaux d'IL-1β, d'IL-6, d'IL-18 et de TNF-α dans le groupe témoin, cet effet était atténué dans le groupe knock-out EIF2AK2. L'examen histologique via la coloration H&E du tissu hépatique a indiqué que l'effet amélioré du BBR sur l'infiltration de l'inflammation hépatique était affaibli chez les souris knock-out EIF2AK2. Ces résultats suggèrent que le BBR régule potentiellement à la baisse la sécrétion d'IL-1β, d'IL-6, d'IL-18 et de TNF-α en ciblant EIF2AK2 et affiche une bonne sécurité.
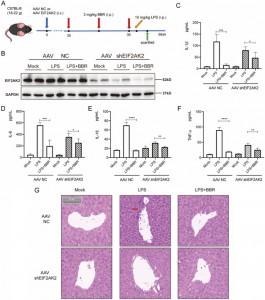
Figure 6 : Vérifications fonctionnelles d’EIF2AK2 in vivo.
Cette étude démontre pleinement les puissants avantages de la technologie ABPP pour élucider les mécanismes complexes des molécules bioactives comme la berbérine, propulsant ainsi l’avancement de la recherche moderne sur les médicaments traditionnels. En découvrant de nouvelles cibles et mécanismes d'action pour l'ancien médicament berbérine, cela enrichit non seulement notre compréhension des fonctions biologiques des médecines traditionnelles, mais ouvre également de nouvelles perspectives et possibilités pour le traitement des maladies liées à l'inflammation. Ce résultat laisse présager qu'avec le soutien de techniques scientifiques modernes telles que l'ABPP, des médicaments plus traditionnels seront réutilisés grâce à l'identification de leurs cibles et mécanismes spécifiques, apportant ainsi une contribution significative aux efforts de santé humaine.
Référence:https://doi.org/10.1016/j.apsb.2022.12.009.
