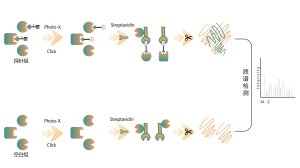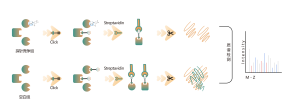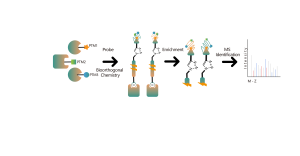Prodotti
Interazioni tra piccole molecole e proteine
Le proteine, in quanto partecipanti diretti ed esecutori delle attività della vita, rappresentano obiettivi cruciali per la terapia delle malattie. I farmaci a piccole molecole (composti organici tipicamente con un peso molecolare inferiore a 1000 Da) esercitano effetti terapeutici efficaci modulando finemente le attività, le abbondanze e le interazioni delle proteine. I comuni farmaci a piccole molecole comprendono prodotti naturali e loro derivati (ad esempio, monomeri vegetali) nonché farmaci sintetizzati chimicamente. Entrando nel corpo umano, questi farmaci esercitano i loro effetti terapeutici legandosi alle proteine bersaglio all’interno delle cellule o all’esterno. Pertanto, comprendere come i farmaci a piccole molecole si legano alle proteine bersaglio è particolarmente cruciale nello sviluppo di farmaci, soprattutto in ambienti fisiologici complessi come cellule viventi, sangue e tessuti malati. L'analisi approfondita dell'interazione tra farmaci di piccole molecole e proteine non solo consente l'identificazione precisa dei bersagli dei farmaci, ma rivela anche i meccanismi molecolari dell'azione dei farmaci e i potenziali effetti fuori bersaglio. Inoltre, mantiene la promessa di scoprire nuovi bersagli terapeutici, fornendo così strategie più ricche per il trattamento delle malattie.
Oltre ai farmaci a piccole molecole, i metaboliti endogeni a piccole molecole presenti negli organismi, come ATP, colesterolo, acidi biliari, acido arachidonico e acido retinoico, partecipano alla regolazione di molte importanti vie di segnalazione e attività proteiche interagendo con le proteine, comprese le proteine di trasporto, le vie di segnalazione e le attività delle proteine. recettori, fattori di trascrizione ed enzimi metabolici. Negli ultimi anni, l’interazione tra i metaboliti del microbiota intestinale e le cellule ospiti è emersa come un punto caldo della ricerca. Pertanto, lo studio approfondito e la mappatura delle reti di interazione tra metaboliti e proteine negli ambienti cellulari, soprattutto negli stati patologici, sono di significativa importanza per comprendere i processi vitali e curare le malattie.
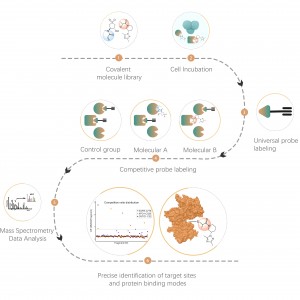
La proteomica chimica, in quanto ramo importante della biologia chimica, è stata ora ampiamente utilizzata nella ricerca sulla funzione delle proteine, nell'identificazione di bersagli di farmaci di piccole molecole e nello screening della nuova struttura dei farmaci. Questa piattaforma tecnologica utilizza una varietà di sonde chimiche funzionalmente diverse, combinate con la proteomica, con l'obiettivo di chiarire i meccanismi di interazione tra piccole molecole e proteine in condizioni fisiologiche (come cellule viventi, sangue, tessuti, ecc.). Vale la pena ricordare che, rispetto ai sistemi proteici purificati, l'uso di sistemi cellulari viventi è una caratteristica importante della proteomica chimica. Consente una rappresentazione realistica della distribuzione dei bersagli per farmaci a piccole molecole, metaboliti endogeni, ecc., all'interno di proteomi complessi, anche fino al livello dei siti dei residui di amminoacidi.
Chomix offre servizi di analisi professionale per le interazioni di piccole molecole-proteine, consentendoti di approfondire i potenziali bersagli farmacologici e di migliorare la tua comprensione dei meccanismi molecolari dei farmaci e dei potenziali effetti collaterali. Il nostro team di esperti possiede una vasta esperienza nella ricerca sulla proteomica chimica e selezionerà per voi i metodi più adatti e affidabili, eliminando qualsiasi preoccupazione relativa alle sfide tecniche e facilitando l'avanzamento della vostra ricerca senza sforzo.

Servizio tecnico
1. Identificazione di bersagli diretti per farmaci a piccole molecole non covalenti
La maggior parte dei farmaci a piccole molecole interagiscono con le proteine bersaglio attraverso legami non covalenti, formando interazioni dinamiche e reversibili con i residui di amminoacidi nelle tasche leganti tramite legami idrogeno, impilamento π-π, interazioni idrofobiche, ecc. Pertanto, l'arricchimento stabile e l'isolamento delle proteine legate da i farmaci a piccole molecole non covalenti provenienti da proteomi complessi pongono sfide significative. Per risolvere questo problema, Chomix ha sviluppato una piattaforma di identificazione dei bersagli di proteomica chimica basata su fotosonde. Questa piattaforma cattura accuratamente il legame dinamico tra piccole molecole e proteine nelle cellule viventi e ottiene la separazione e l'arricchimento, identificando così in modo completo bersagli diretti per farmaci di piccole molecole non covalenti a livello proteomico.
2. Identificazione delle tasche di legame per farmaci a piccole molecole non covalenti
Nel processo di sviluppo di farmaci a piccole molecole, è fondamentale determinare innanzitutto le informazioni di legame tra il farmaco e la proteina, quindi specificare a quale particolare tasca sulla superficie della proteina si lega il farmaco e come si lega. Queste informazioni sono essenziali per la successiva ottimizzazione della struttura del farmaco. Oltre agli approcci classici di biologia strutturale, Chomix ha anche sviluppato una piattaforma tecnologica avanzata di proteomica chimica basata sulla spettrometria di massa ad alta risoluzione. Questa piattaforma è in grado di identificare peptidi leganti per farmaci di piccole molecole non covalenti a livello proteico e persino cellulare, aiutando così ad affrontare questo problema critico nelle prime fasi dello sviluppo del farmaco.
3. Analisi quantitativa dell'occupazione e della selettività dei bersagli farmacologici costituiti da piccole molecole covalenti
I farmaci covalenti si riferiscono a farmaci che formano legami covalenti stabili con residui di amminoacidi nelle tasche leganti delle proteine bersaglio, come quelle che si legano a cisteina, lisina, serina, ecc. I farmaci covalenti comuni includono aspirina, osimertinib, zebularina e prodotti naturali come artemisinina e artesunato. Nelle cellule viventi, i farmaci covalenti possono legarsi stabilmente e occupare specifici residui di amminoacidi sulle proteine bersaglio. Sfruttando questa caratteristica, Chomix ha sviluppato con successo una piattaforma di proteomica chimica basata su una sonda universale. Questa piattaforma consente l'analisi quantitativa dell'occupazione del sito target per i farmaci covalenti a piccole molecole, fino al livello dei residui aminoacidici. Inoltre, analizzando le informazioni sull'occupazione di oltre 10.000 siti di residui di aminoacidi, è possibile determinare la selettività del target a diverse concentrazioni di farmaci, fornendo una guida potente per lo sviluppo iniziale del farmaco.
4. Identificazione e analisi di selettività dei bersagli del degradatore proteico
Essendo un nuovo tipo di farmaco, le chimere mirate alla proteolisi (PROTAC) differiscono dai tradizionali inibitori o attivatori di piccole molecole. Sovvertono il concetto convenzionale di sviluppo “guidato dall’occupazione” in chimica farmaceutica utilizzando il sistema endogeno ubiquitina-proteasoma (UPS) per degradare specificamente le proteine che causano malattie, in particolare quelle considerate obiettivi “non resistenti”. Pertanto, l'identificazione quantitativa dei bersagli dei farmaci degradatori delle proteine e la loro selettività a livello dell'intero proteoma è cruciale per lo sviluppo iniziale di tali farmaci. Chomix ha sviluppato con successo varie piattaforme tecnologiche di proteomica chimica quantitativa in grado di analizzare qualitativamente e quantitativamente oltre 5.000 proteine in singole linee cellulari, fornendo un'analisi completa e approfondita della selettività del bersaglio.