伝統医学の新たな治療的展望:ABPPテクノロジーがベルベリンの新規抗炎症標的EIF2AK2を明らかに
活性ベースのタンパク質プロファイリング(ABPP)などの高度な技術がこれまで知られていなかった治療メカニズムに光を当てるにつれて、伝統医学は新たな薬理学的応用によって活性化しつつあります。これに関連して、ABPP 技術は最近、伝統的な中国の薬用植物から抽出され、中国では一般にコプチシンまたは黄蓮として知られる化合物であるベルベリンの新規抗炎症標的を明らかにしました。この発見は、EIF2AK2がベルベリンの抗炎症作用の重要な役割を担っていることを明らかにし、炎症関連疾患の治療におけるベルベリンの使用に新たな道を切り開きます。この画期的な進歩は、現代の科学的手法を通じて伝統的な医薬品を再利用し、最適化できる可能性を強調しています。

ベルベリンは、抗炎症、低血糖、心血管保護などの幅広い薬理効果を持つ伝統的なアルカロイドであり、かなりの注目を集めています。しかし、特に炎症抑制におけるその正確な分子機構は依然として不明である。
この研究は、ABPP テクノロジーを使用してこの知識のギャップを埋め、ベルベリンが抗炎症作用に関与する重要な標的として EIF2AK2 を特定しました。この発見は、ベルベリンのメカニズムについての理解を深め、ベルベリンの位置付けを変更し、EIF2AK2 を標的とする新しい抗炎症薬を開発するための科学的根拠を提供します。
研究チームは、高度な化学プロテオミクス手法を利用してベルベリンと細胞内タンパク質の相互作用を体系的に調査し、ベルベリンのEIF2AK2への特異的結合とその酵素活性の調節を確認した。これは炎症反応経路に影響を与え、炎症の進行を効果的に阻害します。この重要な進歩は、ベルベリンの抗炎症メカニズムに関する洞察を提供し、EIF2AK2 を標的とする新規治療法の開発をサポートします。
ChomiX は、ABPP や CETSA などの最先端のサービスを提供して、研究者による薬物メカニズムの探索や新薬開発の取り組みの促進を支援します。
研究ルート
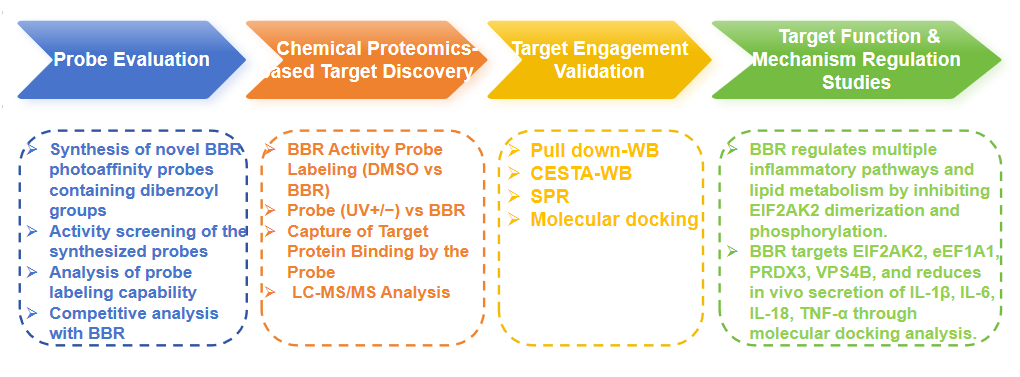
実験プロセス
1. プローブ 11b はプロテオミクス研究における機能ツールとして使用されました。
著者らは、LPS + ナイジェリシン活性化 THP-1 マクロファージ内にジベンゾイル基を含む新規 BBR 光親和性プローブを合成し、スクリーニングしました。これらの中で、化合物 7a および 11b は、IL-1β 発現に対して時間依存性および用量依存性の阻害効果を示し、親化合物 BBR と比較して有効性の向上を示しました。活性ベースのタンパク質プロファイリング (ABPP) 分析と蛍光スキャンを通じて、7a と 11b の両方が標的タンパク質に効果的に結合し、競合阻害を示すことが実証され、BBR と同様の作用機序が示されました。化合物 11b は 2.5% ~ 25% の濃度範囲内で、特に蛍光シグナルの変化が最も顕著である 20 ミリモルの濃度で蛍光強度の顕著な変化を示したという観察に基づいて、プロテオミクス研究用の機能性プローブとして選択されました。 。この選択は、プロテオミクス環境におけるタンパク質相互作用の解明に適したその優れた応答性に基づいています。
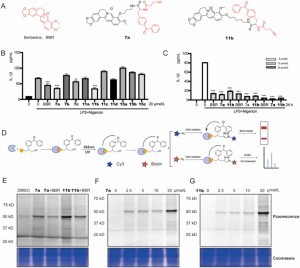
図 1: BBR プローブのスクリーニングと評価。
2. 新規プローブ 11b は、THP-1 細胞内の BBR の 44 個の炎症関連標的タンパク質を同定し、EIF2AK2、eEF1A1、PRDX3、および VPS4B が BBR と特異的な相互作用を持つ直接標的であることを明らかにしました。
著者らは、一連の実験を通じて、新規プローブ 11b を使用して、THP-1 細胞内の潜在的な標的タンパク質をタグ付けして精製することに成功しました。これに続いて、彼らはLC-MS/MS分析を利用して、分子量範囲20〜80 kDaの44の炎症関連タンパク質を同定し、そのうち6つがBBRの抗炎症作用において重要な役割を果たす可能性があることが判明した。さらなる研究により、EIF2AK2、eEF1A1、PRDX3、および VPS4B が BBR の直接の標的であることが確認され、高濃度の BBR 処理下で競合阻害効果を示しました。この発見は、これらのタンパク質とBBRの間に特異的な相互作用が存在する可能性が高いことを明らかにし、それによって、抗炎症過程における薬剤との関与についての新たな洞察が解明された。
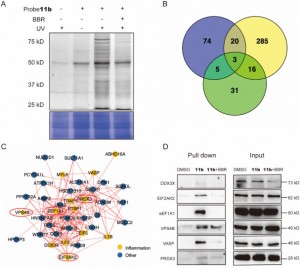
図 2: 標的タンパク質の捕捉と機能解析。
3. 構造生物学の研究により、BBR がどのように EIF2AK2 二量体化を調節し、重要なイオン相互作用やカチオンとパイの結合を通じて抗炎症効果を発揮するかが解明されています。
著者らは、CETSA、SPR、および分子ドッキング技術を利用して、HEK-293 細胞における BBR と 4 つのタンパク質 (EIF2AK2、eEF1A1、PRDX3、および VPS4B) との相互作用を検証しました。結果は、BBR がこれら 4 つのタンパク質の熱安定性を高め、EIF2AK2 に対して最も強い親和性が観察されたことを示しました。さらなる調査により、BBRのEIF2AK2への結合は、主に空洞IIのD316およびE367を含むイオン対、ならびにK291との陽イオン-π相互作用に依存していることが明らかになった。この結合部位はEIF2AK2二量体化に関与しており、BBRがEIF2AK2二量体化を調節することによって抗炎症効果を発揮する可能性があることが示唆されている。
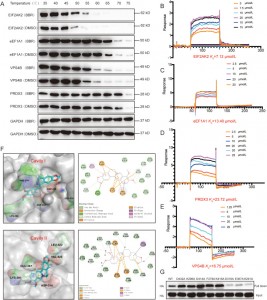
図 3: BBR とその潜在的なターゲット間の親和性研究。
4. 炎症および脂質代謝経路における BBR の役割は、BBR が EIF2AK2 の二量体化とリン酸化を阻害することで明らかになり、それによって NLRP3 インフラマソーム、NF-kB p65/JNK/SIRT1 シグナル伝達の調節において極めて重要な機能を示します。
免疫沈降実験により、BBRがEIF2AK2の二量体化を阻害し、EIF2AK2の自己リン酸化とその基質eIF2aのリン酸化の両方に影響を与えることが確認され、BBRがNLRP3インフラマソーム、NF-kB p65、JNKシグナル伝達経路、SIRT1発現を調節し、細胞の炎症反応において重要な役割を果たしていることが明らかになった。脳の抗炎症メカニズム(アルツハイマー病)、脂肪酸誘発性小胞体ストレス。さらに、EIF2AK2のサイレンシングまたは過剰発現により、p-JNKおよびSIRT1に対するBBRの調節効果が大幅に変化し、BBRがEIF2AK2への結合を介して作用して炎症関連脂質代謝障害を調節することがさらに実証された。
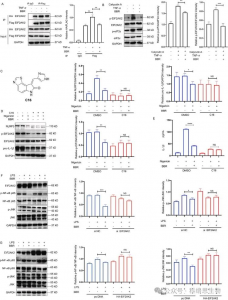
図 2 標的タンパク質の捕捉と機能解析。
5. EIF2AK2、eEF1A1、PRDX3、および VPS4B を標的とすることで、BBR は複数の炎症経路を調整し、EIF2AK2 はこれらの標的の中で支配的な制御役割を果たします。
この相互作用をさらに調査するために、著者らは4つのタンパク質の過剰発現およびノックダウンモデルを確立し、BBRがJNK、NF-kB、MAPK、およびAKT炎症経路を選択的に調節し、EIF2AK2が主要な役割を果たすことを実証し、これはin vivo実験で検証された。 。
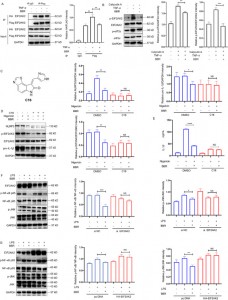
図 5: BBR 標的タンパク質の機能研究
6. EIF2AK2 の特異的標的化を通じて、BBR は、IL-1β、IL-6、IL-18、および TNF-α の生体内分泌を下方制御します。 EIF2AK2 遺伝子をノックダウンすると、その抗炎症効果と肝臓保護作用が減少します。
次に彼らは、in vivoでEIF2AK2を標的とすることにより、BBRがIL-1β、IL-6、IL-18、およびTNF-α放出に影響を与えるかどうかを調査した。そうするために、彼らは、shEIF2AK2を保有するアデノ随伴ウイルス(AAV)の静脈内注射を使用して、EIF2AK2遺伝子ノックアウトマウスモデルを作成しました。野生型およびEIF2AK2ノックアウトマウスにBBR(3mg/kg)を腹腔内投与し、続いてLPS注射を行った。 BBR は対照群では IL-1β、IL-6、IL-18、および TNF-α のレベルを有意に低下させましたが、この効果は EIF2AK2 ノックアウト グループでは減弱されました。肝組織の H&E 染色による組織学的検査により、EIF2AK2 ノックアウト マウスでは肝炎症浸潤に対する BBR の改善効果が弱まっていることが示されました。これらの発見は、BBR が EIF2AK2 を標的とすることによって IL-1β、IL-6、IL-18、および TNF-α の分泌を潜在的に下方制御し、良好な安全性を示すことを示唆しています。
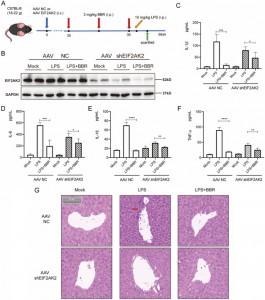
図 6: EIF2AK2 の in vivo 機能検証。
この研究は、ベルベリンのような生理活性分子の複雑なメカニズムを解明する上での ABPP テクノロジーの強力な利点を十分に実証し、伝統的な薬物に関する現代の研究の進歩を推進します。古い薬であるベルベリンの新しい標的と作用機序を明らかにすることで、伝統薬の生物学的機能についての理解が深まるだけでなく、炎症関連疾患の治療に対する新たな視点と可能性も開かれます。この結果は、ABPP などの現代科学技術の支援により、より伝統的な薬物がその特定の標的とメカニズムの特定を通じて再利用され、人類の健康への取り組みに大きく貢献することを予感させます。

