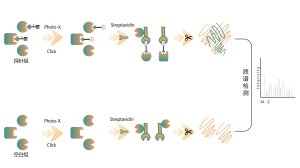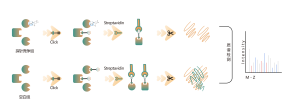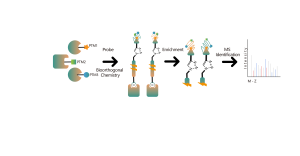製品
共有結合性低分子医薬品のタンパク質標的の競合的ケモプロテオミクスプロファイリング
プラットフォームの技術的特徴
非共有結合性薬剤と同様に、レポーター基で官能化された化学プローブを使用することによるダイレクトプルダウン戦略も、共有結合性小分子薬剤について成功裡に実証されている。ただし、一部の共有結合性薬物は、生物活性の損失または合成不可能なため、化学修飾に耐えられないことは注目に値します。さらに、形成された共有結合は通常、MS 検出中は不安定です。
競合的ケモプロテオミクス戦略は理想的な代替手段であり、タンパク質標識に普遍的な活性ベースのプローブを使用します。システイン、リジン、セリン、ヒスチジン残基と反応する特異的な化学プローブが開発されました。原則として、アミノ酸残基は、共有結合性小分子によって占有されると、プローブによって標識することができなくなります。その結果、この競合戦略によりアミノ酸の分解能によりONターゲットとOFFターゲットを網羅的に同定することができた。

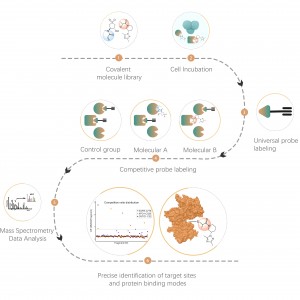
ワークフロー

このプラットフォームは構造化されたワークフローに従い、共有結合分子による生細胞の標識から始まり、標識プロテオーム抽出、化学プローブ標識、生体直交ライゲーション、ストレプトアビジンベースの濃縮、プロテアーゼ消化、同位体標識、最終的な質量分析検出などのステップが続きます。
ケーススタディ
プロジェクトの目的
アムジェン社が開発した AMG510 は、腫瘍における KRAS-G12C 変異を標的とする初めて承認された薬剤です。このプロジェクトの目的は、KRAS-G12C 変異を持つ NCI-H358 細胞における AMG510 のオンおよびオフターゲットをプロファイリングすることでした。

実験方法
ChomiX の中核テクノロジー プラットフォームの 1 つである DIA-ABPP を使用して、プロテオーム レベルでのターゲット占有率を分析しました。
データの視覚化



NCI-H358 細胞では、5768 個のタンパク質から合計 16992 個の Cys 部位が定量されました。 KRAS_C12部位の標的占有率は、1μM AMG510の処理下で100%に近かった。現場で一方、他のサイト KRAS_C80 は影響を受けませんでした。このデータは、AMG510 の高い標的特異性を実証しました。 (標識されたCys残基は*で示されます)