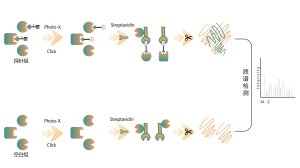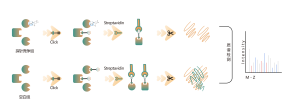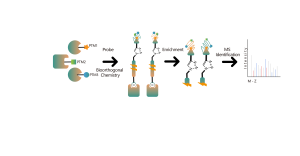製品
低分子とタンパク質の相互作用
タンパク質は、生命活動の直接の参加者および実行者として、疾患治療の重要な標的となります。低分子薬 (通常、分子量が 1000 Da 未満の有機化合物) は、タンパク質の活性、存在量、相互作用を細かく調節することで効果的な治療効果を発揮します。一般的な小分子薬には、天然物とその誘導体 (ハーブモノマーなど)、および化学合成薬が含まれます。これらの薬剤は人体に入ると、細胞内または細胞外の標的タンパク質に結合することで治療効果を発揮します。したがって、小分子薬が標的タンパク質にどのように結合するかを理解することは、創薬、特に生細胞、血液、病変組織などの複雑な生理学的環境において特に重要です。小分子薬物とタンパク質間の相互作用を詳細に分析することで、薬物標的の正確な同定が可能になるだけでなく、薬物作用の分子機構や潜在的なオフターゲット効果も明らかになります。さらに、新たな治療標的を発見し、それによって疾患治療のためのより豊富な戦略を提供できる可能性を秘めています。
小分子薬に加えて、ATP、コレステロール、胆汁酸、アラキドン酸、レチノイン酸などの生物体内の内因性小分子代謝産物は、輸送タンパク質、膜などのタンパク質と相互作用することにより、多くの重要なシグナル伝達経路およびタンパク質活性の調節に関与しています。受容体、転写因子、代謝酵素など。近年、腸内微生物叢の代謝物と宿主細胞との相互作用が研究のホットスポットとして浮上しています。したがって、細胞環境、特に病気の状態における代謝物とタンパク質の間の相互作用ネットワークを徹底的に調査し、マッピングすることは、生命プロセスを理解し、病気を治療するために非常に重要です。
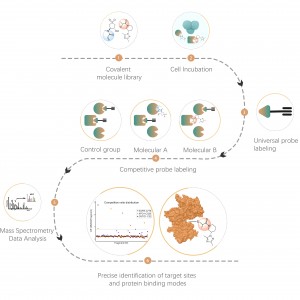
ケミカルプロテオミクスは、ケミカルバイオロジーの重要な分野として、現在、タンパク質機能研究、小分子薬物標的の同定、および新しい薬物構造のスクリーニングに広く採用されています。この技術プラットフォームは、機能的に多様な化学プローブをプロテオミクスと組み合わせて利用し、生理学的条件(生細胞、血液、組織など)下での小分子とタンパク質の間の相互作用メカニズムを解明することを目的としています。精製タンパク質システムと比較して、生細胞システムの使用が化学プロテオミクスの主要な特徴であることは言及する価値があります。これにより、複雑なプロテオーム内の低分子薬剤、内因性代謝産物などの標的の分布を、アミノ酸残基部位のレベルに至るまで現実的に描写することが可能になります。
Chomix は、小分子とタンパク質の相互作用に関する専門的な分析サービスを提供し、潜在的な薬物標的をさらに深く掘り下げ、薬物の分子メカニズムと潜在的な副作用についての理解を深めることができるようにします。当社の専門家チームは化学プロテオミクス研究における豊富な経験を有しており、お客様にとって最も適した信頼性の高い手法を選択し、技術的な課題に関する懸念を解消し、お客様の研究を容易に進めることができます。

テクニカルサービス
1. 非共有結合性低分子薬の直接標的の同定
ほとんどの小分子医薬品は非共有結合を通じて標的タンパク質と相互作用し、水素結合、π-πスタッキング、疎水性相互作用などを介して結合ポケット内のアミノ酸残基と動的かつ可逆的な相互作用を形成します。複雑なプロテオームからの非共有結合性小分子薬は、重大な課題を引き起こします。これに対処するために、Chomix はフォトプローブに基づいた化学プロテオミクス ターゲット識別プラットフォームを開発しました。このプラットフォームは、生細胞内の小分子とタンパク質間の動的な結合を正確に捕捉し、分離と濃縮を実現することで、非共有結合性小分子薬の直接標的をプロテオームレベルで包括的に同定します。
2. 非共有結合性低分子薬物の結合ポケットの同定
低分子医薬品の開発プロセスでは、最初に薬物とタンパク質間の結合情報を決定し、次に薬物がタンパク質表面のどの特定のポケットに結合するのか、またどのように結合するのかを特定することが重要です。この情報は、その後の薬物構造の最適化に不可欠です。古典的な構造生物学的アプローチに加えて、Chomix は高分解能質量分析に基づく高度な化学プロテオミクス技術プラットフォームも開発しました。このプラットフォームは、非共有結合性小分子薬剤の結合ペプチドをタンパク質レベル、さらには細胞レベルで同定できるため、初期の薬剤開発におけるこの重要な問題への対処に役立ちます。
3. 共有結合性小分子薬物標的の占有率と選択性の定量分析
共有結合性薬剤とは、システイン、リジン、セリンなどに結合するものなど、標的タンパク質上の結合ポケットのアミノ酸残基と安定した共有結合を形成する薬剤を指します。一般的な共有結合性薬剤には、アスピリン、オシメルチニブ、ゼブラリンのほか、次のような天然物が含まれます。アルテミシニンとアルテスネート。生細胞では、共有結合性薬物は標的タンパク質上の特定のアミノ酸残基に安定して結合し、占有することができます。この特性を利用して、チョミックスはユニバーサルプローブに基づく化学プロテオミクスプラットフォームの開発に成功しました。このプラットフォームにより、共有結合性小分子薬剤の標的部位の占有をアミノ酸残基のレベルに至るまで定量的に分析できます。さらに、10,000 を超えるアミノ酸残基部位の占有情報を分析することで、さまざまな薬物濃度での標的選択性を決定でき、初期の薬物開発に強力なガイダンスを提供します。
4. タンパク質分解物質標的の同定と選択性分析
新しいタイプの薬剤であるタンパク質分解ターゲティングキメラ (PROTAC) は、従来の小分子阻害剤や活性化剤とは異なります。彼らは、内因性ユビキチンプロテアソームシステム(UPS)を利用して疾患の原因となるタンパク質、特に「治療不可能な」標的と考えられているタンパク質を特異的に分解することにより、医薬品化学における従来の「占有駆動型」開発概念を覆します。したがって、タンパク質分解剤の薬物標的とその選択性をプロテオーム全体レベルで定量的に同定することは、そのような薬物の早期開発にとって極めて重要です。 Chomix は、個々の細胞株の 5,000 を超えるタンパク質を定性的および定量的に分析できるさまざまな定量的化学プロテオミクス技術プラットフォームの開発に成功し、標的選択性の包括的かつ詳細な分析を提供します。