[높은 점수 돌파] 새로운 억제제 AJ 2-30을 사용한 SLC15A4의 항염증 조절 개선: 화학적 단백질체학 접근법(IF 14.8)
이 기사에서는 화학적 단백질체학을 사용하여 항원 제시 세포에서 고도로 발현되는 중요한 염증성 막횡단 단백질인 SLC15A4를 표적으로 하는 다양한 신규 억제제를 고안하고 선별합니다. 잠재적인 억제제의 초기 표적화는 완전 기능화된 단편(FFF) 프로브 라이브러리 전략을 활용하여 FFF-21을 수많은 프로브 중에서 IFN-α 생산의 강력한 억제제로 식별했습니다. 후속 구조 최적화를 통해 화합물 AJ 2-30이 개발되었으며, 이는 탁월한 억제를 입증했을 뿐만 아니라 SLC15A4가 광가교 후 변형의 주요 표적임을 확인했습니다. 추가 조사에 따르면 AJ 2-30은 SLC15A4 안정성을 감소시키고 리소좀 경로를 통해 분해를 유도하며 TLR 7-9 및 NOD의 활성화를 효과적으로 억제함으로써 강력한 항염증 효과를 발휘하는 것으로 나타났습니다. 이 연구는 상당한 항염증 활성을 갖는 SLC15A4 억제제를 성공적으로 개척했을 뿐만 아니라 새로운 항염증제 개발의 길을 열었습니다.

연구 경로
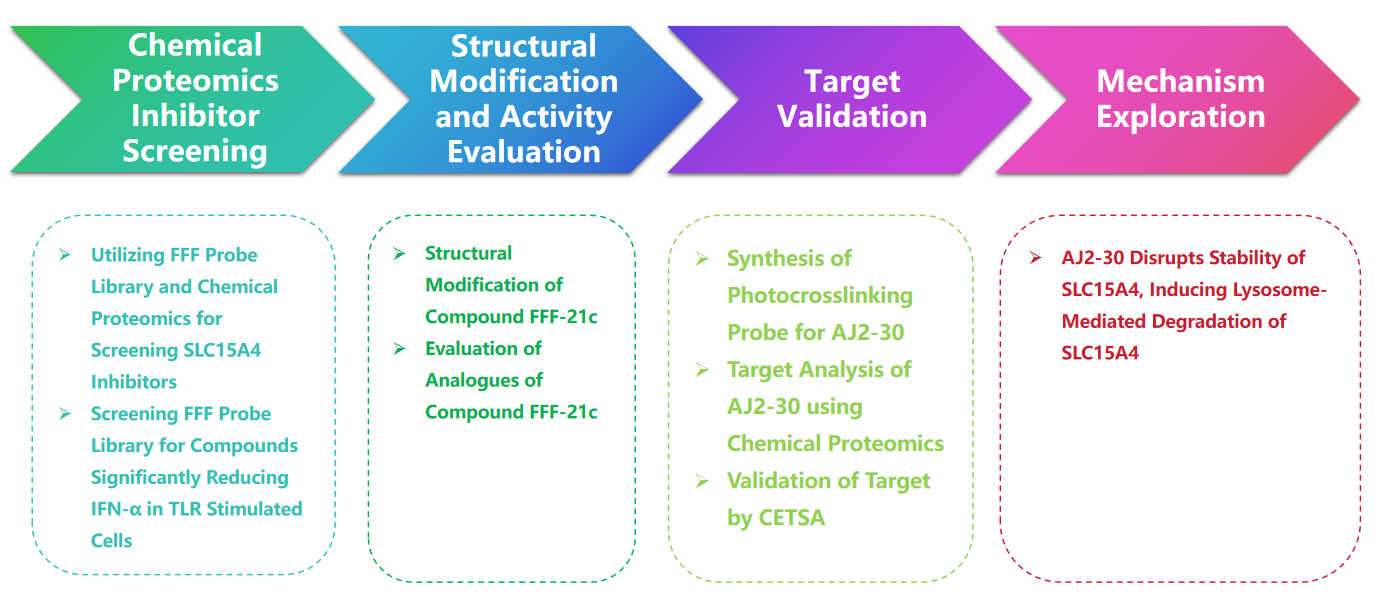
실험 과정
1. SLC15A4 억제제를 스크리닝하기 위한 완전 기능화된 단편(FFF) 프로브 라이브러리 전략.
저자는 FFF(완전히 기능화된 단편) 프로브 라이브러리를 사용하여 SLC15A4 억제제를 스크리닝함으로써 연구를 시작했습니다. 이 FFF는 SLC15A4를 표적으로 삼도록 설계된 정제 조각을 포함하는 분자 인식 그룹 하나와 SLC15A4를 시각화하기 위한 이중 아크리미딘 및 알킨 그룹을 특징으로 하는 또 다른 사진 가교 농축 그룹의 두 가지 구성 요소로 구성됩니다. 저자들은 화학적 단백질체학 작업 흐름을 사용하여 이 FFF 프로브 라이브러리가 세포 내 SLC15A4에 결합하는 것을 확인하고 FFF 프로브가 TLR 9 자극 세포에서 IFN-α 수준을 약화시킬 수 있는지 여부를 평가했습니다. 결과는 SLC15A4에 결합하는 모든 FFF 프로브 중에서 FFF-21이 IFN-α 수준을 억제하는 가장 높은 능력을 나타냈으며, 라벨이 없는 유사체인 FFF-21c도 유사한 억제 효과를 나타냄을 보여주었습니다.
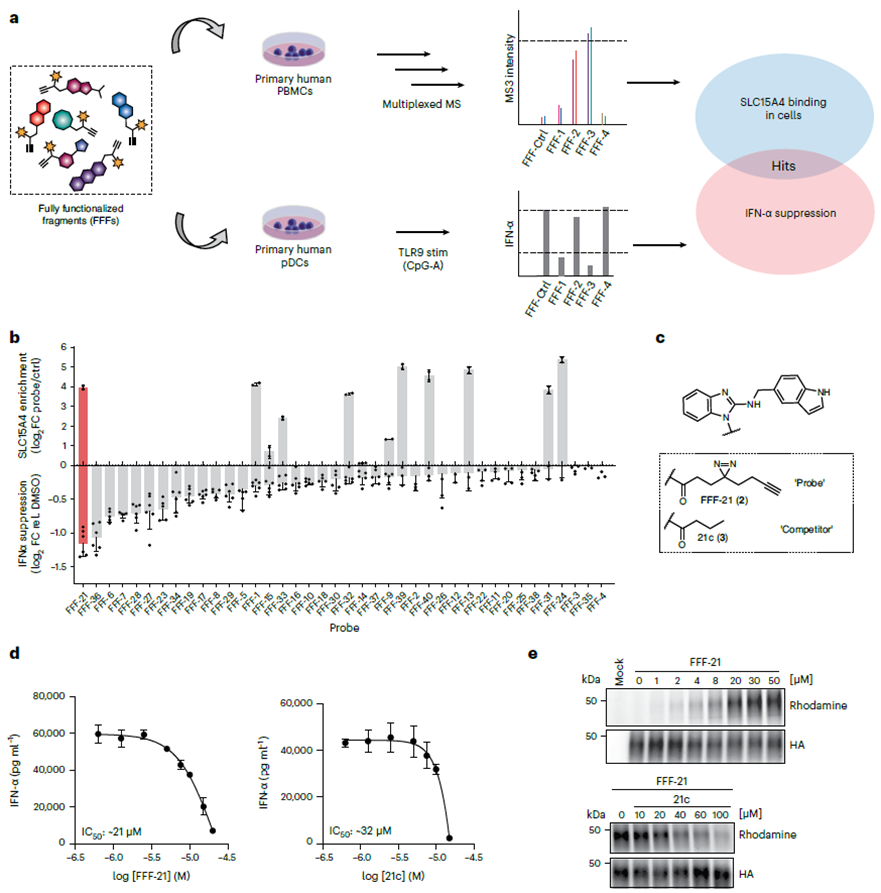
2. SLC15A4 억제제의 광가교 결합 변형.
화합물 FFF-21c의 초기 선택 이후, 저자는 그 구조를 최적화하는 작업을 진행했습니다. FFF-21c의 여러 유사체 합성을 통해 그들은 AJ 2-30이 가장 강력한 억제제임을 확인했습니다. 광가교 기술을 사용하여 표적과의 상호 작용을 확인했습니다. 그 후, ABPP의 직접 라벨링 방법과 간접 경쟁 방법을 CETSA(세포 열 이동 분석)와 함께 활용하여 저자는 SLC15A4를 AJ 2-30의 주요 표적으로 확정했습니다.
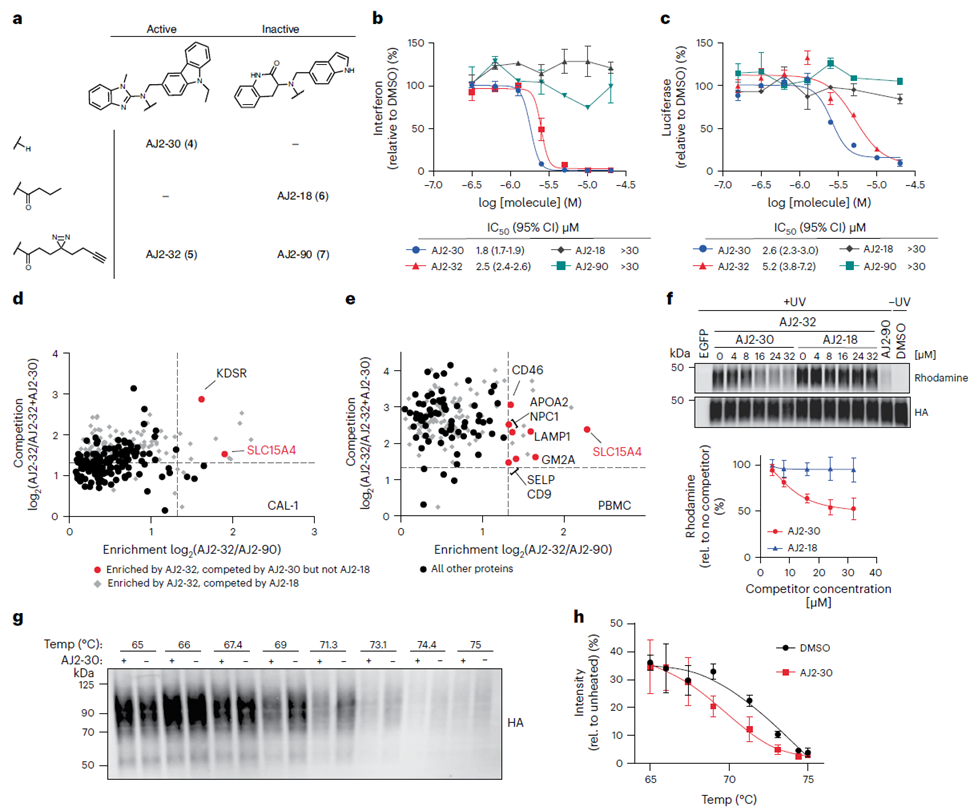
3. 항염증 메커니즘은 AJ 2-30이 SLC15A4 안정성을 방해한다는 것을 보여줍니다.
AJ 2-30의 SLC15A4 결합 및 억제 효과를 확인한 후, 저자들은 AJ 2-30의 항염증 메커니즘을 밝히기 위해 일련의 생화학적 실험을 수행했습니다. 결과는 AJ 2-30이 단백질을 불안정화함으로써 SLC15A4의 리소좀 매개 분해를 유도함으로써 SLC15A4 의존 방식으로 면역 세포에서 TLR 7-9 및 NOD의 활성화를 억제한다는 것을 보여주었습니다. 이는 염증성 질환 및 자가면역 질환 치료에 있어 AJ 2-30의 잠재력을 강조합니다.
요약하면, 이 연구는 뛰어난 항염증 활성을 갖는 강력한 SLC15A4 억제제인 AJ 2-30을 식별하기 위해 화학적 단백질체학 기술을 적절하게 활용합니다. 이 화합물은 SLC15A4 안정성과 항원 제시 및 염증 신호 전달 경로에서의 역할을 구체적으로 표적으로 삼아 동물 모델에서 상당한 효능을 입증합니다. 이러한 중추적인 발전은 항염증 치료 표적에 대한 이해를 향상시킬 뿐만 아니라 다양한 염증 및 자가면역 질환에 대한 새로운 치료제 개발을 위한 강력한 기반을 마련합니다. 추가 연구와 임상 검증을 통해 이 새로운 SLC15A4 억제제는 다수의 환자에게 보다 정확하고 효과적인 치료 옵션을 제공함으로써 전 세계 건강에 중대한 영향을 미칠 준비가 되어 있습니다.

