기술적 배경
화학적 단백질체학 기술은 변화의 신호탄으로 등장하여 정제된 단백질에서 벗어나 살아있는 세포의 영역으로 약물 발견을 유도합니다.
화학적 단백질체학 기술은 살아있는 세포 내에서 소분자-단백질 상호작용을 조사하는 것을 특징으로 하는 강력한 약물 발견 플랫폼 역할을 합니다. 당사의 공유 약물 발견 플랫폼 중 하나는 시스테인 잔기의 티올 그룹과의 공유 반응을 통해 단백질 표적과 결합하는 공유 결합제를 발견하도록 설계되었습니다. 기존의 단일 표적 스크리닝 전략과 달리 화학적 단백질체학 플랫폼은 친전자성 단편과 살아있는 세포의 거의 모든 단백질 간의 상호작용을 아미노산 잔기 분해능으로 정량 분석할 수 있습니다. 10,000개 이상의 단백질에 대한 적용 범위를 자랑하며,여러 포유동물 세포주에서 ~40,000개의 시스테인 부위(잠재적인 약물 결합 부위).

작업흐름
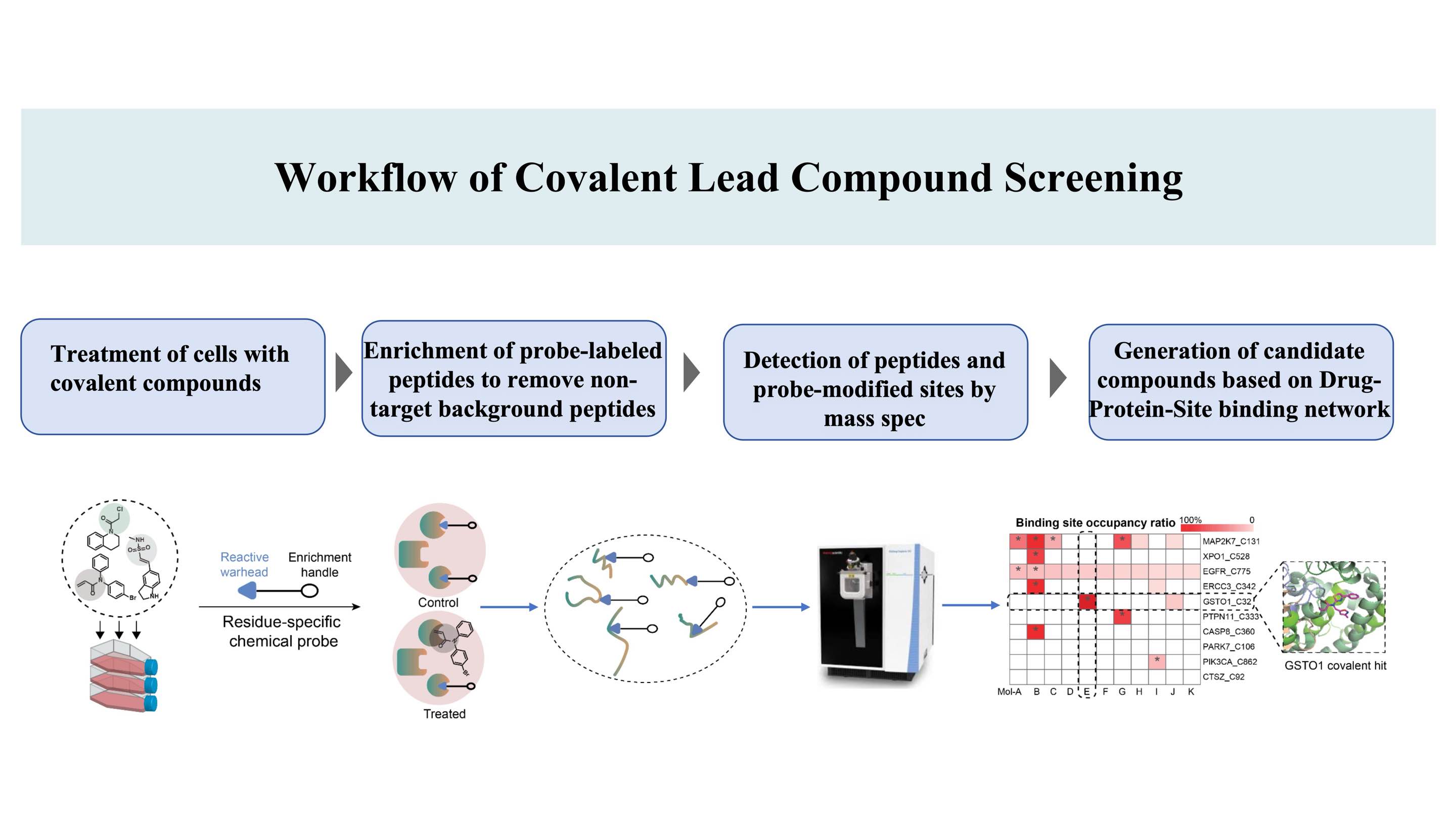
DIA-ABPP(Data-Independent Acquisition-Activity-Based Protein Profiling) 특허(공유 결합 부위는 화학적 프로브로 표지할 수 있는 아미노산입니다. 이로써 리간드 가능성을 가능하게 함)
기술적 장점
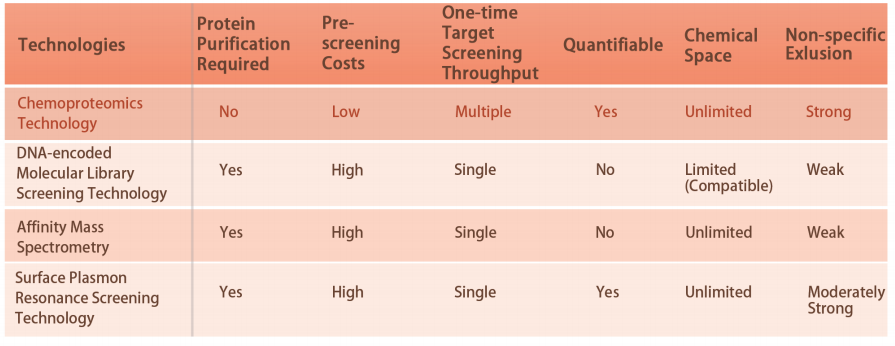
특징 1
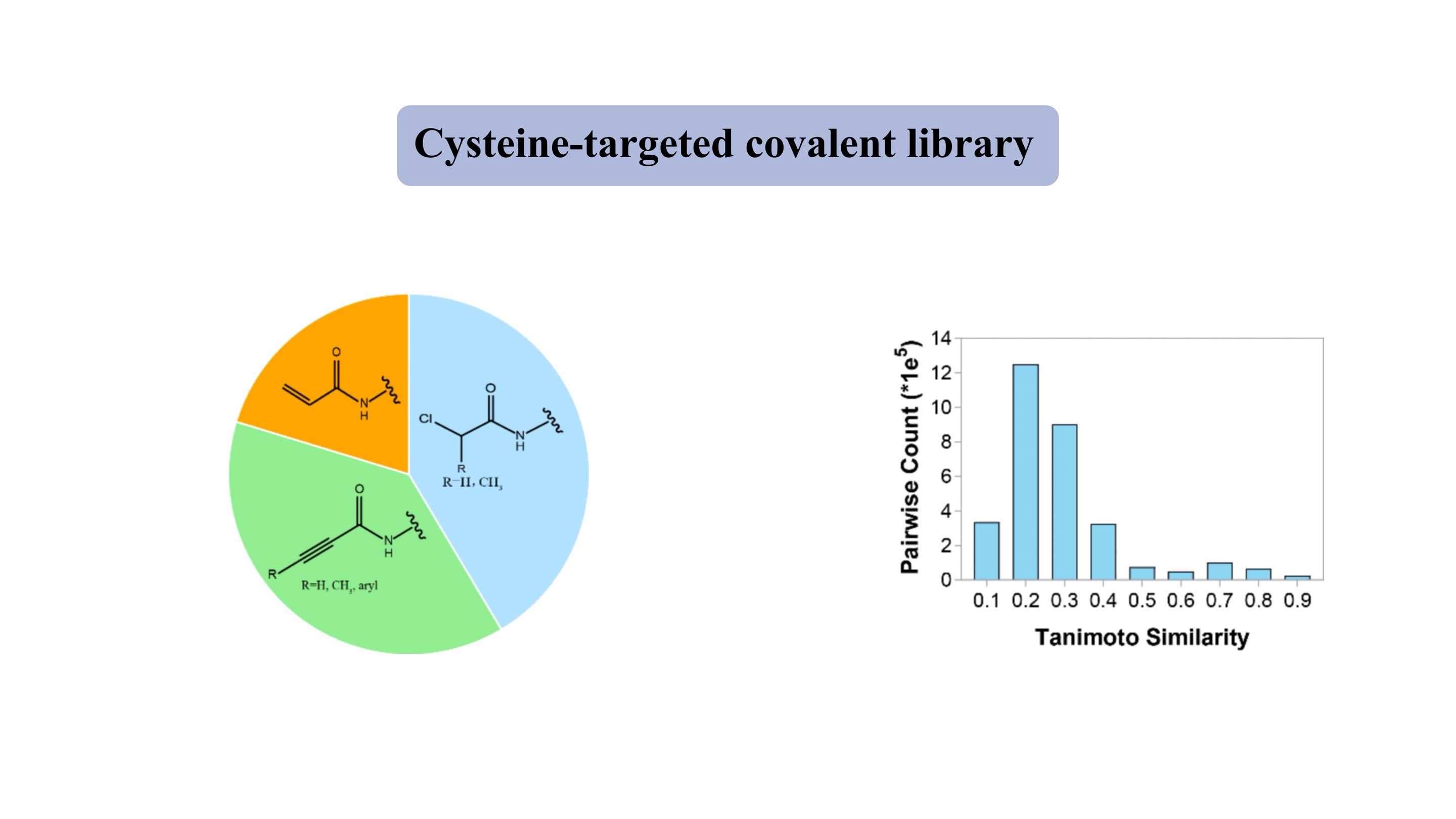
시스테인 표적 공유 라이브러리
시스테인 표적 공유 결합 라이브러리에는 아크릴아미드 및 클로로아세트아미드와 같은 대표적인 약한 친전자성 "탄두"가 포함되어 있습니다. "약물 유사" 라이브러리에는 약 3000개의 화합물이 포함되어 있으며, 그 중 80% 이상이 300-500 Da의 분자량을 나타냅니다. 대부분의 화합물의 경우 Tanimoto 유사성 지수는 구성원 두 개당 약 0.3으로, 이는 높은 다양성을 나타냅니다.
특징 2
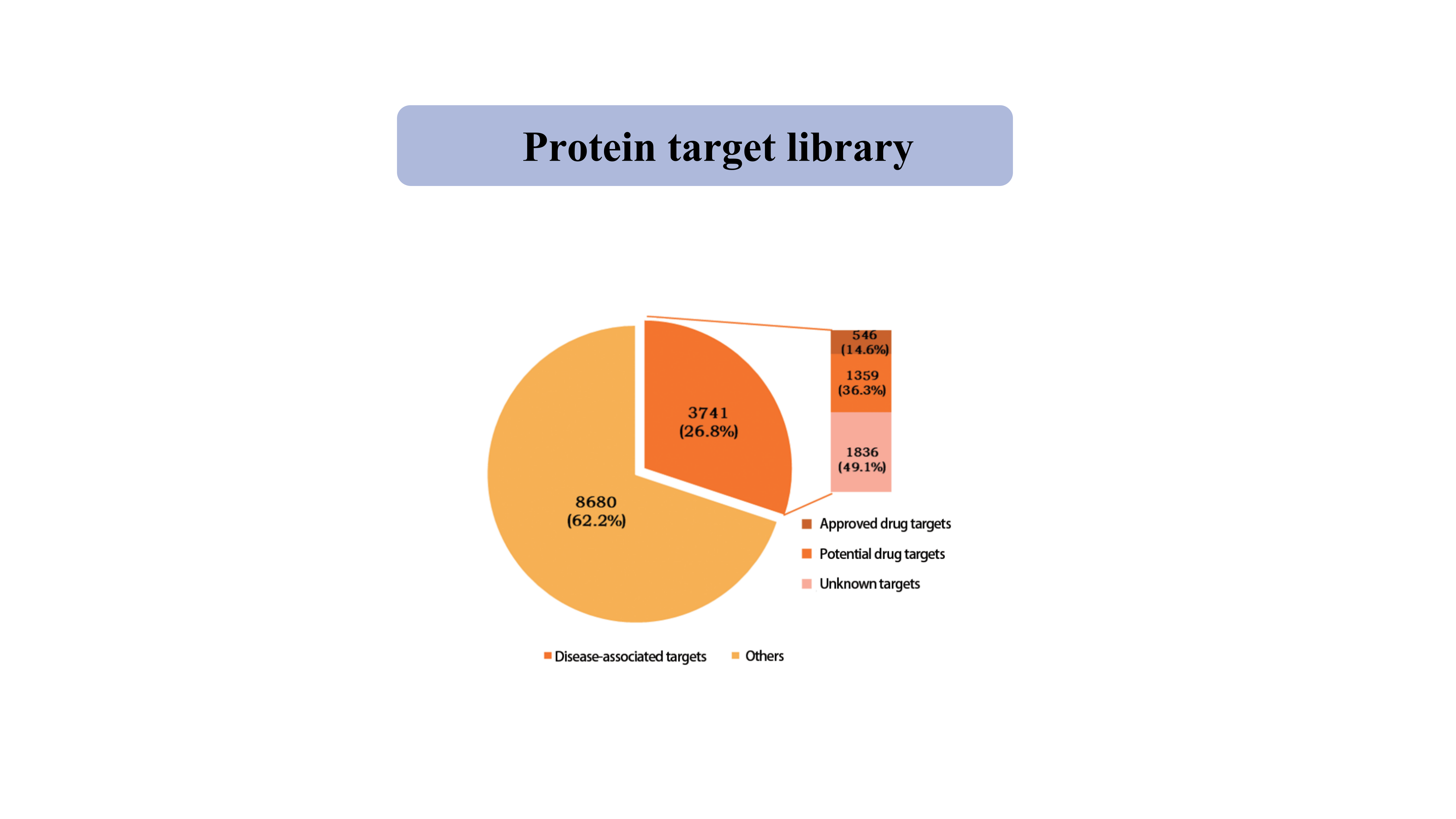
단백질 표적도서관
현재 티올 특이적 화학 프로브에 의해 포착된 단백질 표적 라이브러리는 키나제, 포스파타제, 리가제 및 전사 인자를 포함하여 12421개 단백질의 39962개 시스테인 부위를 포괄합니다.
사례 연구
DCAF1은 두 가지 E3 리가제(CRL4DCAF1 및 EDVP)에 대한 기질 수용체 역할을 하며 단백질 분해에 중요한 생리학적 역할을 합니다. DCAF1의 WDR 도메인을 표적으로 하는 여러 공유 및 비공유 결합제는 표적화된 분해 적용을 지원하기 위해 개발되었습니다(Targeted Protein Degradation by Electrophilic PROTACs which Stereoselectively and Site-Specifically Engage DCAF1. J. Am. Chem. Soc. 2022, 144, 40, 18688) –18699. 임상적으로 검증된 표적에 대해 활동하는 DCAF1 기반 PROTAC 내재적 및 후천적 분해자 저항 극복 Nat. 2024, 15, 275.
우리는 Mol-380이 DCAF1_C69와 공유 결합하여 WDR 도메인과 별개로 TPD 응용 프로그램을 위한 잠재적인 약품 가능 사이트로 강조된다는 사실을 처음으로 발견했습니다. 우리의 연구 결과는 전사 인자 및 막 단백질을 포함하여 살아있는 세포에서 다루기 어려운 표적에 대한 새로운 리간드를 발견하는 데 있어 ChomiX 자동화 화학 단백질체학 플랫폼의 중요한 가치를 강조하고, 약물 개발 및 기능 탐색에 대한 잠재적인 영향을 강조합니다.
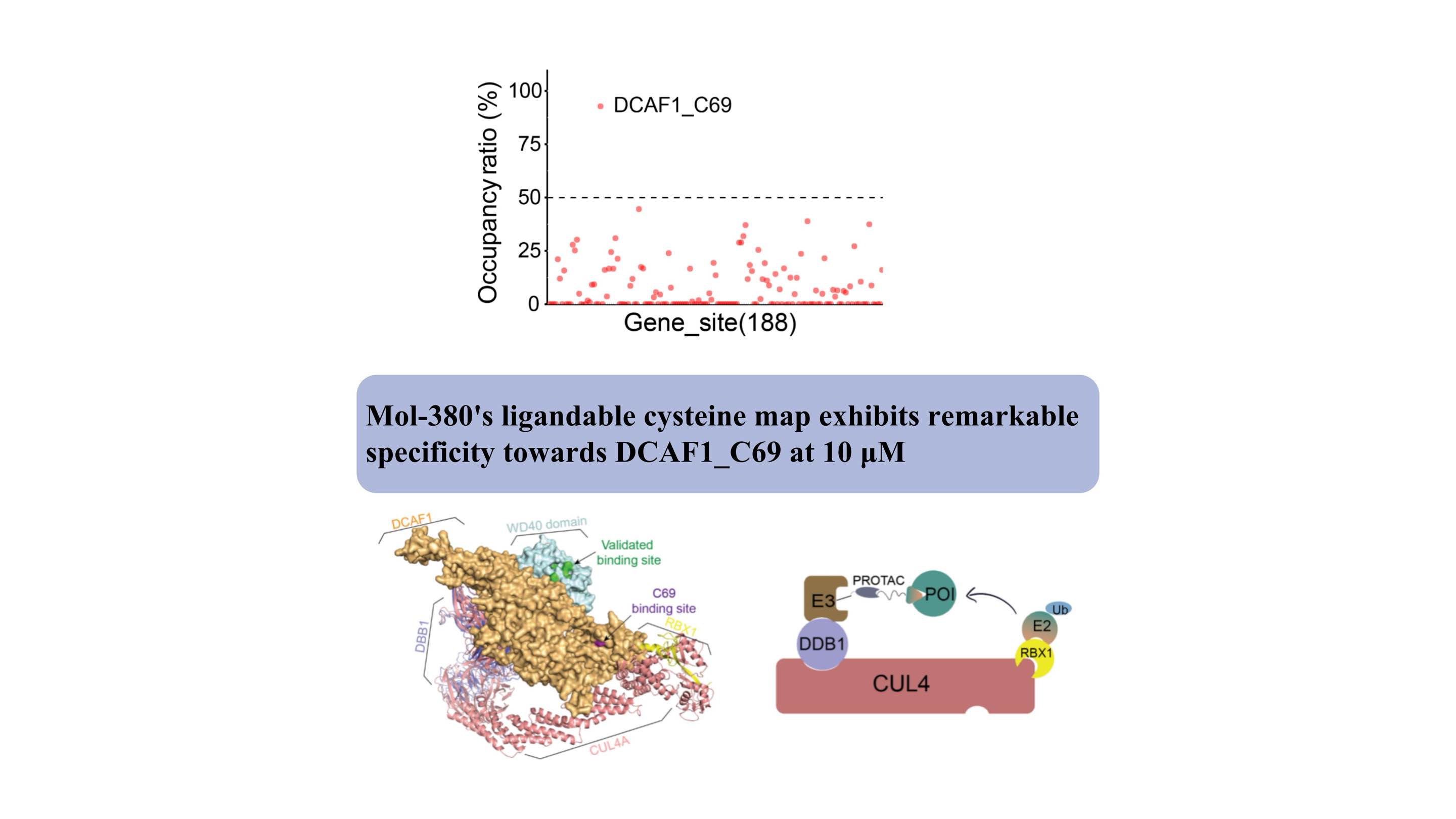
구조적으로 C69의 결합 사이트는 복잡한 모델에서 알 수 있듯이 WD40 도메인의 검증된 포켓에 인접해 있으며 PROTAC 개발을 위한 새로운 사이트를 제공합니다.

