기술 플랫폼
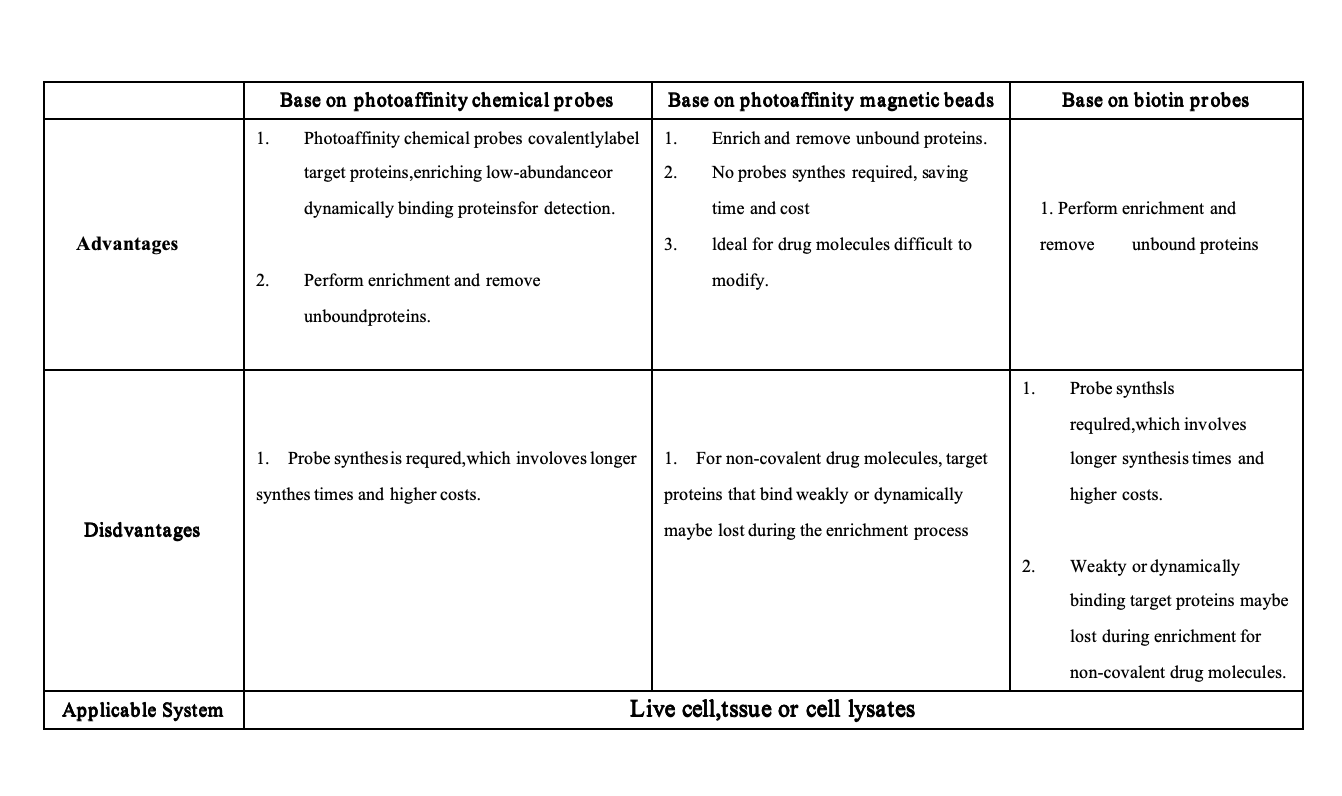
Chemoproteomics는 특히 화학 프로브 기반 플랫폼을 통해 약물 표적 발견을 발전시켰습니다. 그러나 복잡한 합성, 낮은 수율, 높은 비용 및 약물 분자의 알려지지 않은 SAR과 같은 과제는 진행을 방해합니다.
광친화성 자기 비드 플랫폼은 UV 조명을 통해 활성 약물 분자를 기능성 자기 비드에 고정함으로써 이러한 문제를 해결하므로 화학적 프로브 설계가 필요하지 않습니다. 이는 약물과 표적 단백질 사이의 특정 결합을 보장합니다. 프로테옴과 함께 인큐베이션한 후 비드는 약물 표적 단백질을 농축하고 분리한 다음 면역블로팅 및 질량 분석법으로 분석합니다.
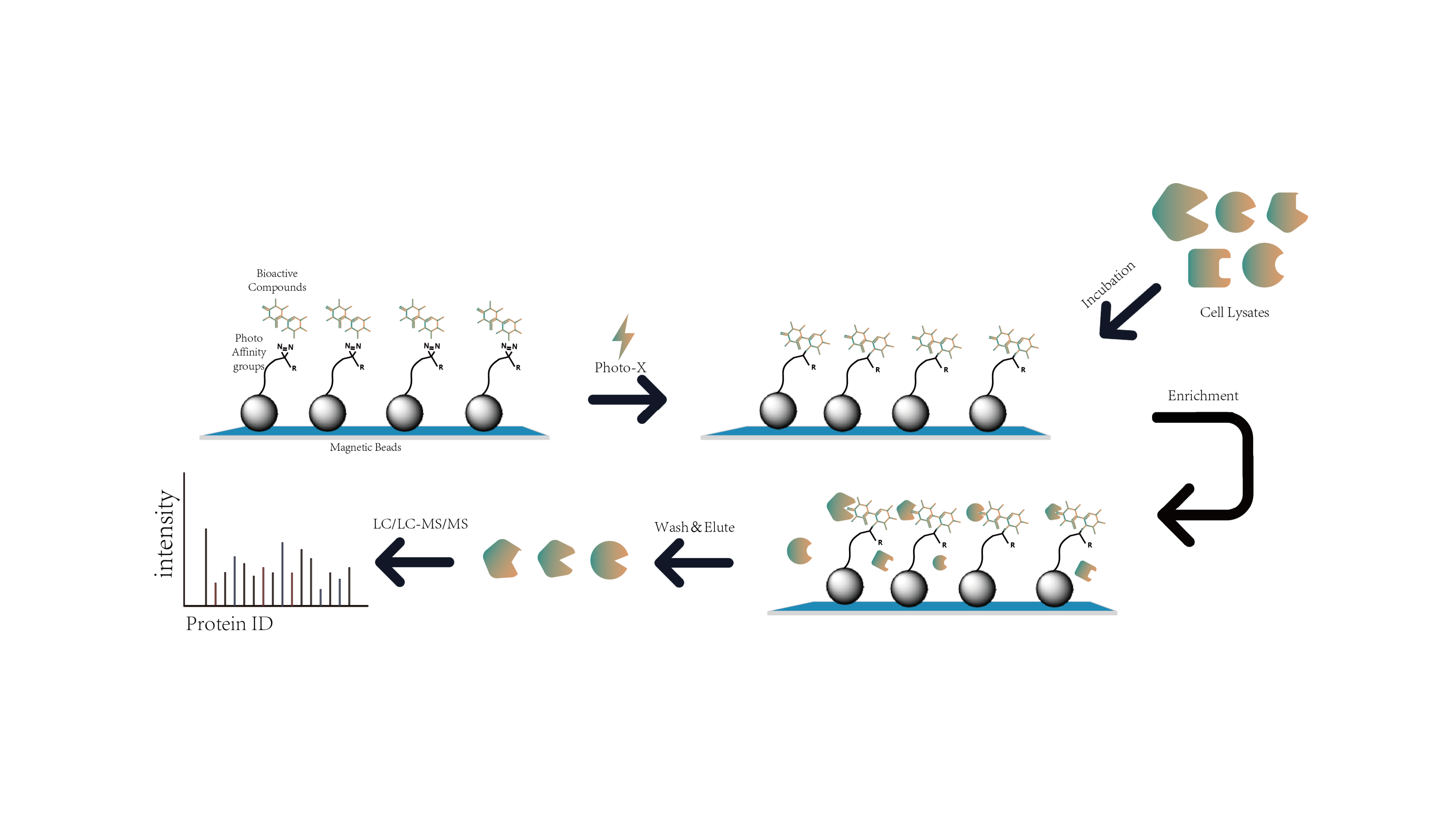
플랫폼 기능
사례 연구
스타우로스포린(Stau)의 표적을 검증하기 위해 우리는 이를 광친화성 변형 기능성 자기 비드(Stau-beads)의 표면에 고정시켰습니다. 그 후, 우리는 Fmoc-beads를 대조군으로 사용하여 Stau-beads를 전체 프로테옴과 함께 배양했습니다. 결과적인 웨스턴 블롯(WB) 결과는 아래 그림에 표시되어 있으며, 이는 Stau-beads가 표적 단백질 FECH(알려진 양성 표적)를 효과적으로 농축했음을 나타냅니다.
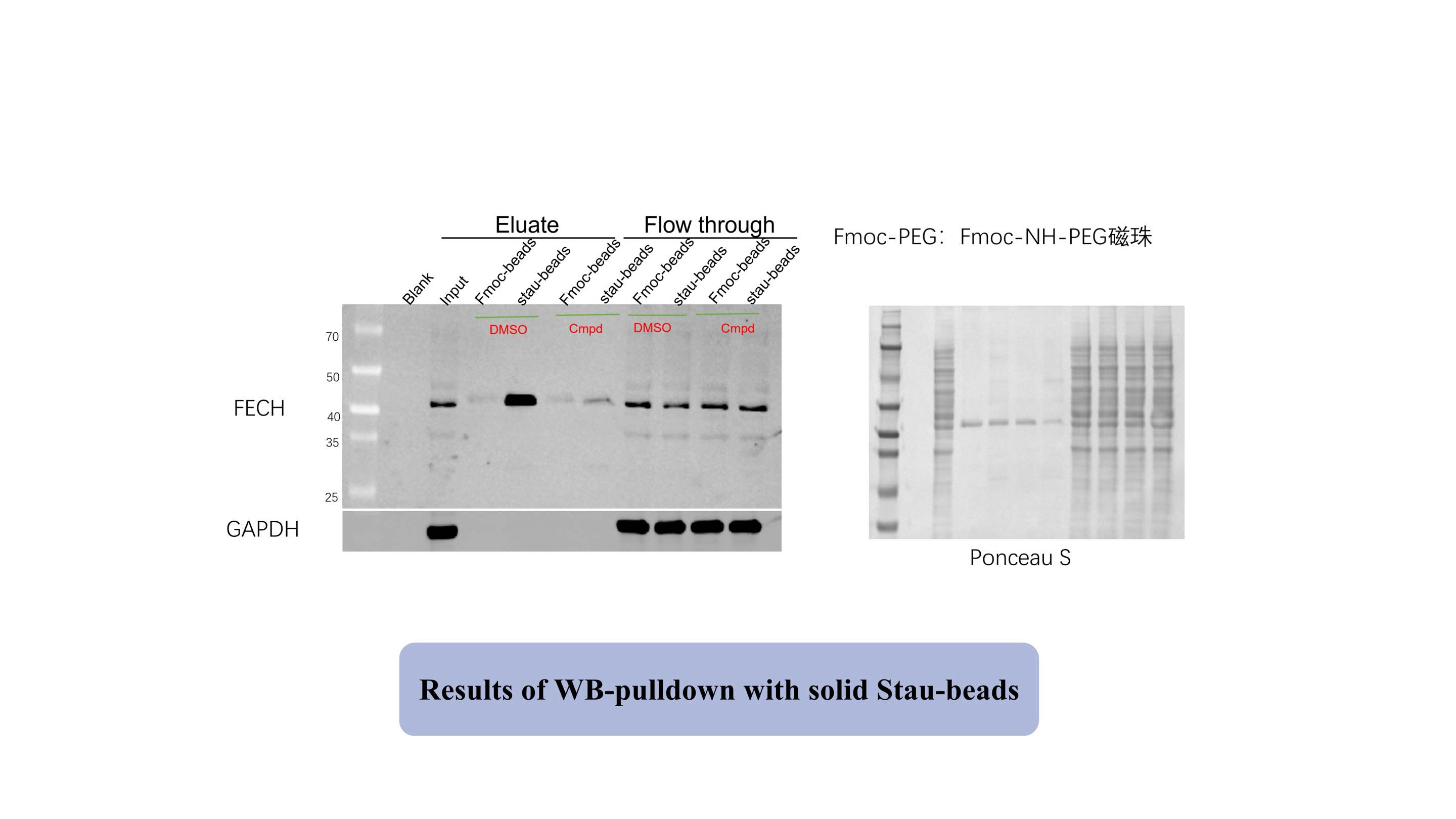
다음으로, Fmoc-beads와 Stau-beads를 사용하여 농축 및 분리된 단백질을 효소분해 및 질량분석법 분석을 실시했습니다. 실험군(Stau-beads)과 대조군(Fmoc-beads)의 단백질 강도 차이를 정량적으로 비교했습니다. 결과는 알려진 모든 양성 표적 단백질이 Stau-beads 그룹에서 상당히 풍부하다는 것을 보여주어 방법의 효율성을 확인시켜 주었습니다.