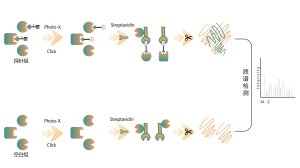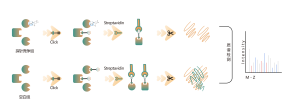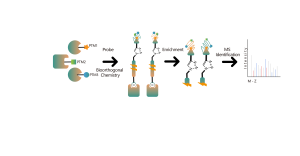Producten
Kwantitatieve analyse van bezetting en selectiviteit van covalente geneesmiddeldoelen voor kleine moleculen
Covalente geneesmiddelen werken voornamelijk door het vormen van covalente bindingen met specifieke aminozuurresiduen op doeleiwitten, zoals cysteïne, lysine en serine. Aspirine is een van de vroegst bekende covalente medicijnmoleculen. Bovendien vertonen veel natuurlijke producten covalente eigenschappen, zoals oridonine, dat ontstekingsremmende bioactiviteit heeft. De afgelopen jaren hebben covalente gerichte geneesmiddelen steeds meer aandacht gekregen van farmaceutische bedrijven. Tot op heden zijn ten minste zes covalente geneesmiddelen die zich richten op kinasen goedgekeurd door de FDA, waaronder ibrutinib, dat zich richt op de BTK-kinase.
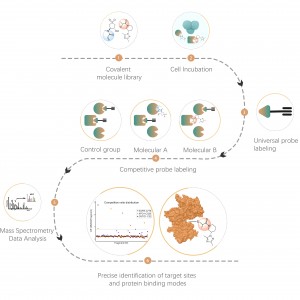
Bij de ontdekking van covalente medicijndoelen in cellen of weefsels is een effectieve strategie de chemische modificatie van actieve kleine moleculen door het introduceren van reportergroepen (zoals biotine of bioorthogonale groepen). Deze modificatie maakt, terwijl de oorspronkelijke activiteit van het molecuul behouden blijft, de directe vangst van op elkaar inwerkende eiwitdoelen in levende cellen of weefsels mogelijk. Veel actieve moleculen zijn echter moeilijk chemisch te modificeren, of de producten die worden gevormd na reactie met aminozuurresiduen zijn onstabiel, waardoor ze ongeschikt zijn voor massaspectrometriedetectie. Om deze uitdagingen het hoofd te bieden, biedt ChomiX een oplossing: identificatie van de modificatieplaats met behulp van competitieve labeling met aminozuurspecifieke probes.
Technisch platform
Ons technologieplatform is gecentreerd rond een universele aminozuurspecifieke chemische sonde. Wanneer een actief klein molecuul reageert met een aminozuurresidu en de bindingsplaats bezet, genereert deze universele chemische probe een significant signaalverschil voor die bindingsplaats vergeleken met blanco controlemonsters. Door deze verschillen in de labelingssignalen te detecteren, kunnen we nauwkeurig informatie verkrijgen over de doeleiwitten en aminozuurresiduen van het actieve molecuul, inclusief zowel verwachte (on-target) als potentiële off-target eiwitten. Dit technologieplatform biedt robuuste ondersteuning voor doelontdekking van covalente geneesmiddelen en onderzoek naar werkingsmechanismen van geneesmiddelen.

Onze voordelen
1. Technische uitmuntendheid: ervaren team, publicaties in tijdschriften van topniveau en gezaghebbende industriële diensten.
2. Kernoctrooitechnologie: exclusieve patenten en geavanceerde hardware voor ondersteuning in de vroege ontwikkeling van geneesmiddelen.
3. One-stop-service: omvat sondeontwerp, synthese, doeldetectie, bio-informatica-analyse en tijdige voortgangsfeedback voor klanttevredenheid.
4. Rigoureus kwaliteitsmanagement: ISO9001-certificering zorgt voor betrouwbare en authentieke rapporten.
Onze service
| Project | Kwantitatieve analyse van bezetting en selectiviteit van covalente geneesmiddeldoelen voor kleine moleculen |
| Steekproef | Zuiver eiwit, cellysaat, levende cellen, ziek weefsel, bloed, bacteriën, plantenweefsel |
| Hardwareplatform | Contactloze ultrasone celvergruizer, ChemiDoc MP Imaging System, Orbitrap Fusion Lumos Tribrid/Orbitrap Exploris 480/Q Exactive HF-X/timsTOF Pro 2 massaspectrometer |
| Projectduur | 2-4 weken |
| Leveringen | Projectrapport (inclusief experimentele procedures, data-analysegrafieken, bio-informatica-analyseresultaten) |
| Prijs | Klik om te raadplegen |
Casestudy
AMG510, ontwikkeld door Amgen, is 's werelds eerste gerichte medicijn voor KRAS-G12C-mutante tumoren. Dit project heeft tot doel de doelspecificiteit en selectiviteit ervan in overeenkomstige mutante cellen te verifiëren. Met behulp van het DIA-ABPP-platform van Chomix hebben we de covalente doelwitten van AMG510 in cellen uitgebreid gescreend tot op het niveau van aminozuurresiduen.
Experimentele gegevens laten zien dat in vier herhaalde experimenten met NCI-H358-cellen in totaal 16.992 cysteïneresiduen van 5.768 eiwitten systematisch werden geanalyseerd. Onder behandeling met 1 μM AMG510 vertoonde de KRAS_C12-site significante veranderingen, terwijl KRAS_C80 onaangetast bleef, wat sterk bewijs leverde voor de hoge specificiteit van AMG510 ten aanzien van de KRAS-G12C-mutante site (gemarkeerd met een asterisk die de beoogde cysteïneresidu-site aangeeft).