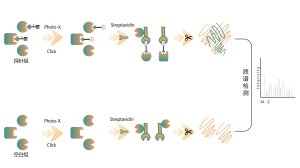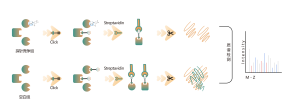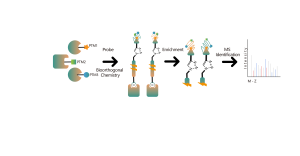Producten
Interacties tussen kleine moleculen en eiwitten
Eiwitten vertegenwoordigen, als directe deelnemers en uitvoerders van levensactiviteiten, cruciale doelwitten voor ziektetherapie. Geneesmiddelen met kleine moleculen (organische verbindingen die doorgaans een molecuulgewicht van minder dan 1000 Da hebben) oefenen effectieve therapeutische effecten uit door de eiwitactiviteiten, -abundanties en -interacties nauwkeurig te moduleren. Veel voorkomende geneesmiddelen met kleine moleculen omvatten natuurlijke producten en hun derivaten (bijvoorbeeld kruidenmonomeren), maar ook chemisch gesynthetiseerde geneesmiddelen. Bij binnenkomst in het menselijk lichaam oefenen deze medicijnen hun therapeutische effecten uit door zich te binden aan doeleiwitten in cellen of extern. Daarom is het begrijpen van hoe kleine molecuulgeneesmiddelen binden aan doeleiwitten bijzonder cruciaal bij de ontwikkeling van geneesmiddelen, vooral in complexe fysiologische omgevingen zoals levende cellen, bloed en zieke weefsels. Een diepgaande analyse van de interactie tussen geneesmiddelen met kleine moleculen en eiwitten maakt niet alleen een nauwkeurige identificatie van de doelwitten van geneesmiddelen mogelijk, maar onthult ook de moleculaire mechanismen van de werking van geneesmiddelen en potentiële off-target-effecten. Bovendien houdt het de belofte in om nieuwe therapeutische doelen te ontdekken, waardoor rijkere strategieën voor de behandeling van ziekten worden geboden.
Naast kleinmoleculaire geneesmiddelen nemen endogene kleinmoleculaire metabolieten in organismen, zoals ATP, cholesterol, galzuren, arachidonzuur en retinoïnezuur, deel aan het reguleren van vele belangrijke signaalroutes en eiwitactiviteiten door interactie met eiwitten, waaronder transporteiwitten, membraaneiwitten en membraaneiwitten. receptoren, transcriptiefactoren en metabolische enzymen. De afgelopen jaren is de interactie tussen metabolieten van de darmmicrobiota en gastheercellen uitgegroeid tot een onderzoekshotspot. Daarom zijn grondig onderzoek en het in kaart brengen van de interactienetwerken tussen metabolieten en eiwitten in cellulaire omgevingen, vooral onder zieke toestanden, van groot belang voor het begrijpen van levensprocessen en het behandelen van ziekten.
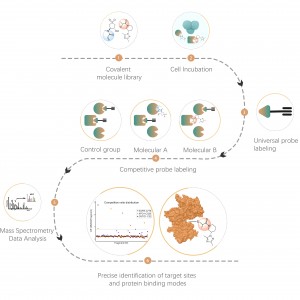
Chemische proteomics worden, als een belangrijke tak van de chemische biologie, nu op grote schaal toegepast bij het onderzoek naar de eiwitfunctie, de identificatie van doelwitten van kleine moleculen en het screenen van nieuwe geneesmiddelenstructuren. Dit technologische platform maakt gebruik van een verscheidenheid aan functioneel diverse chemische probes, gecombineerd met proteomics, met als doel de interactiemechanismen tussen kleine moleculen en eiwitten onder fysiologische omstandigheden (zoals levende cellen, bloed, weefsels, enz.) op te helderen. Het is de moeite waard te vermelden dat, vergeleken met gezuiverde eiwitsystemen, het gebruik van levende celsystemen een belangrijk kenmerk is van chemische proteomics. Het maakt een realistische weergave mogelijk van de verdeling van doelwitten voor geneesmiddelen met kleine moleculen, endogene metabolieten, enz., binnen complexe proteomen, zelfs tot op het niveau van aminozuurresiduplaatsen.
Chomix biedt professionele analysediensten voor interacties tussen kleine moleculen en eiwitten, waardoor u dieper in potentiële geneesmiddeldoelen kunt duiken en uw begrip van de moleculaire mechanismen van geneesmiddelen en mogelijke bijwerkingen kunt vergroten. Ons deskundige team beschikt over uitgebreide ervaring in chemisch proteomisch onderzoek en selecteert voor u de meest geschikte en betrouwbare methoden, waardoor u zich geen zorgen meer hoeft te maken over technische uitdagingen en de voortgang van uw onderzoek moeiteloos kunt vergemakkelijken.

Technische dienst
1. Identificatie van directe doelwitten voor niet-covalente kleine molecuulgeneesmiddelen
De meeste geneesmiddelen met kleine moleculen interageren met doeleiwitten door middel van niet-covalente binding, waarbij ze dynamische en omkeerbare interacties vormen met aminozuurresiduen in bindingsholtes via waterstofbruggen, π-π-stapeling, hydrofobe interacties, enz. Daarom is een stabiele verrijking en isolatie van eiwitten die gebonden zijn door niet-covalente geneesmiddelen met kleine moleculen uit complexe proteomen vormen aanzienlijke uitdagingen. Om dit aan te pakken heeft Chomix een platform voor chemische proteomics-doelidentificatie ontwikkeld op basis van fotosondes. Dit platform legt nauwkeurig de dynamische binding tussen kleine moleculen en eiwitten in levende cellen vast en bereikt scheiding en verrijking, waardoor directe doelen voor niet-covalente kleine molecuulgeneesmiddelen op proteomisch niveau uitgebreid worden geïdentificeerd.
2. Identificatie van bindingszakken voor niet-covalente geneesmiddelen met kleine moleculen
In het proces van de ontwikkeling van kleine moleculen is het van cruciaal belang om eerst de bindingsinformatie tussen het medicijn en het eiwit te bepalen, en vervolgens te specificeren aan welke specifieke pocket op het eiwitoppervlak het medicijn bindt en hoe het bindt. Deze informatie is essentieel voor de daaropvolgende optimalisatie van de geneesmiddelstructuur. Naast de klassieke benaderingen van de structurele biologie heeft Chomix ook een geavanceerd technologieplatform voor chemische proteomics ontwikkeld, gebaseerd op massaspectrometrie met hoge resolutie. Dit platform kan bindende peptiden voor niet-covalente geneesmiddelen met kleine moleculen identificeren op eiwit- en zelfs cellulair niveau, en helpt daarmee bij het aanpakken van dit cruciale probleem bij de vroege ontwikkeling van geneesmiddelen.
3. Kwantitatieve analyse van bezetting en selectiviteit van covalente geneesmiddeldoelen voor kleine moleculen
Covalente geneesmiddelen verwijzen naar geneesmiddelen die stabiele covalente bindingen vormen met aminozuurresiduen op bindingsplaatsen op doeleiwitten, zoals die binden aan cysteïne, lysine, serine, enz. Veel voorkomende covalente geneesmiddelen omvatten aspirine, osimertinib, zebularine, evenals natuurlijke producten zoals artemisinine en artesunaat. In levende cellen kunnen covalente geneesmiddelen stabiel binden aan specifieke aminozuurresiduen op doeleiwitten en deze innemen. Door gebruik te maken van deze eigenschap heeft Chomix met succes een chemisch proteomicsplatform ontwikkeld op basis van een universele sonde. Dit platform maakt kwantitatieve analyse mogelijk van de bezetting van de doellocatie voor covalente geneesmiddelen met kleine moleculen, tot op het niveau van aminozuurresiduen. Bovendien kan het, door de bezettingsinformatie voor meer dan 10.000 locaties met aminozuurresiduen te analyseren, de doelselectiviteit bij verschillende geneesmiddelconcentraties bepalen, wat krachtige richtlijnen biedt voor de vroege ontwikkeling van geneesmiddelen.
4. Identificatie en selectiviteitsanalyse van eiwitafbraakdoelen
Als nieuw type medicijn verschillen Proteolysis Targeting Chimeras (PROTAC's) van traditionele remmers of activatoren van kleine moleculen. Ze ondermijnen het conventionele ‘bezettingsgestuurde’ ontwikkelingsconcept in de medicinale chemie door gebruik te maken van het endogene ubiquitine-proteasoomsysteem (UPS) om specifiek ziekteverwekkende eiwitten af te breken, vooral die welke als ‘niet-mediceerbare’ doelwitten worden beschouwd. Daarom is kwantitatieve identificatie van doelwitten voor eiwitafbrekende geneesmiddelen en hun selectiviteit op het gehele proteoomniveau cruciaal voor de vroege ontwikkeling van dergelijke geneesmiddelen. Chomix heeft met succes verschillende kwantitatieve chemische proteomics-technologieplatforms ontwikkeld die in staat zijn om meer dan 5.000 eiwitten in individuele cellijnen kwalitatief en kwantitatief te analyseren, waardoor een uitgebreide en diepgaande analyse van de doelselectiviteit ontstaat.