[Przełom z wysoką punktacją] Postępowa regulacja przeciwzapalna SLC15A4 z nowatorskim inhibitorem AJ 2-30: podejście do proteomiki chemicznej (IF 14.8)
W tym artykule wykorzystano proteomikę chemiczną do opracowania i przeszukania szeregu nowych inhibitorów ukierunkowanych na SLC15A4, kluczowe białko transbłonowe zapalne, ulegające silnej ekspresji w komórkach prezentujących antygen. Początkowe namierzanie potencjalnych inhibitorów wykorzystywało strategię biblioteki sond w pełni funkcjonalizowanych fragmentów (FFF), identyfikując FFF-21 jako silny inhibitor wytwarzania IFN-α spośród wielu sond. Późniejsza optymalizacja strukturalna doprowadziła do opracowania związku AJ 2-30, który nie tylko wykazał doskonałe hamowanie, ale także potwierdził, że SLC15A4 jest jego główną docelową modyfikacją po fotosieciowaniu. Dalsze badania wykazały, że AJ 2-30 wywiera silne działanie przeciwzapalne, zmniejszając stabilność SLC15A4, indukując jego degradację poprzez szlak lizosomalny i skutecznie hamując aktywację TLR 7-9 i NOD. Badanie to nie tylko z sukcesem pionierskie w zakresie inhibitorów SLC15A4 o znaczącym działaniu przeciwzapalnym, ale także toruje drogę do opracowania nowych leków przeciwzapalnych.

Trasa Badawcza
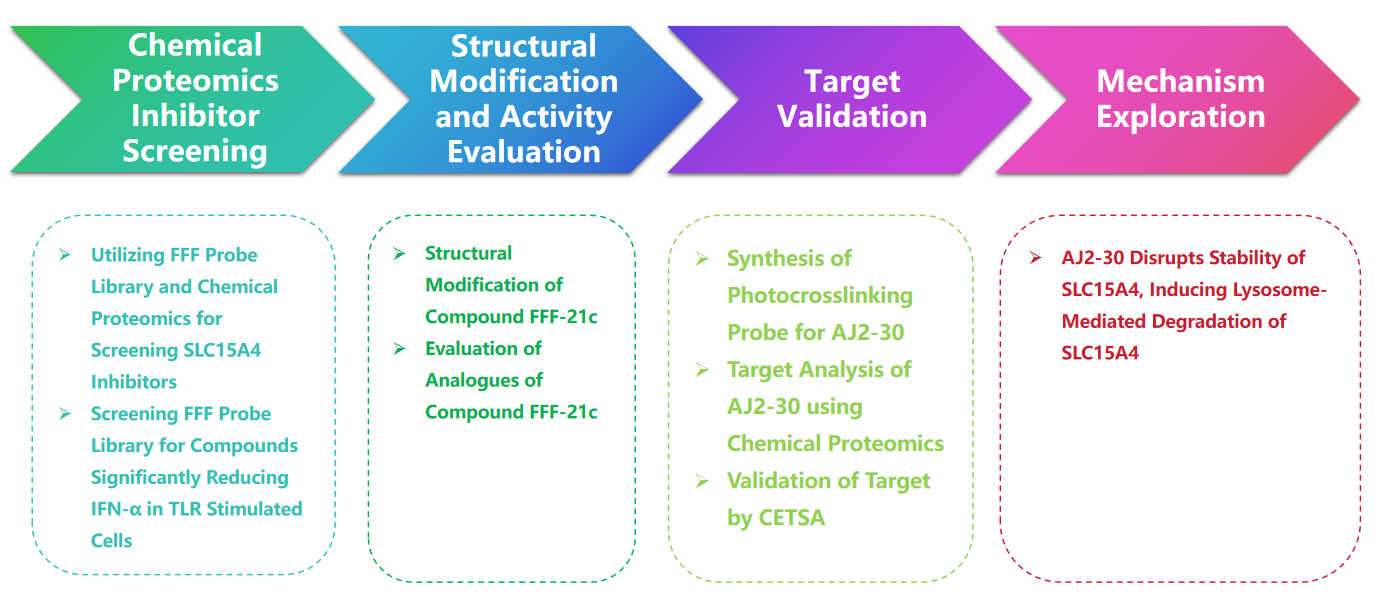
Proces eksperymentalny
1. Strategia biblioteki sond w pełni funkcjonalizowanych fragmentów (FFF) w celu przeszukiwania inhibitorów SLC15A4.
Autorzy rozpoczęli badania od przeszukania inhibitorów SLC15A4 przy użyciu biblioteki sond w pełni funkcjonalizowanych fragmentów (FFF). Ten FFF składa się z dwóch składników: jednej grupy rozpoznawania molekularnego zawierającej fragmenty tabletki zaprojektowanej do celowania w SLC15A4 i innej wzbogaconej grupy fotousieciowanej zawierającej podwójne grupy akrymidynowe i alkinowe w celu wizualizacji SLC15A4. Stosując proces proteomiki chemicznej, autorzy potwierdzili wiązanie tej biblioteki sond FFF z SLC15A4 w komórkach i ocenili, czy sonda FFF może osłabiać poziomy IFN-α w komórkach stymulowanych TLR 9. Wyniki wykazały, że spośród wszystkich sond FFF wiążących się z SLC15A4, FFF-21 wykazywał największą zdolność do hamowania poziomów IFN-α, a jego pozbawiony znacznika analog, FFF-21c, również wykazywał podobne działanie hamujące.
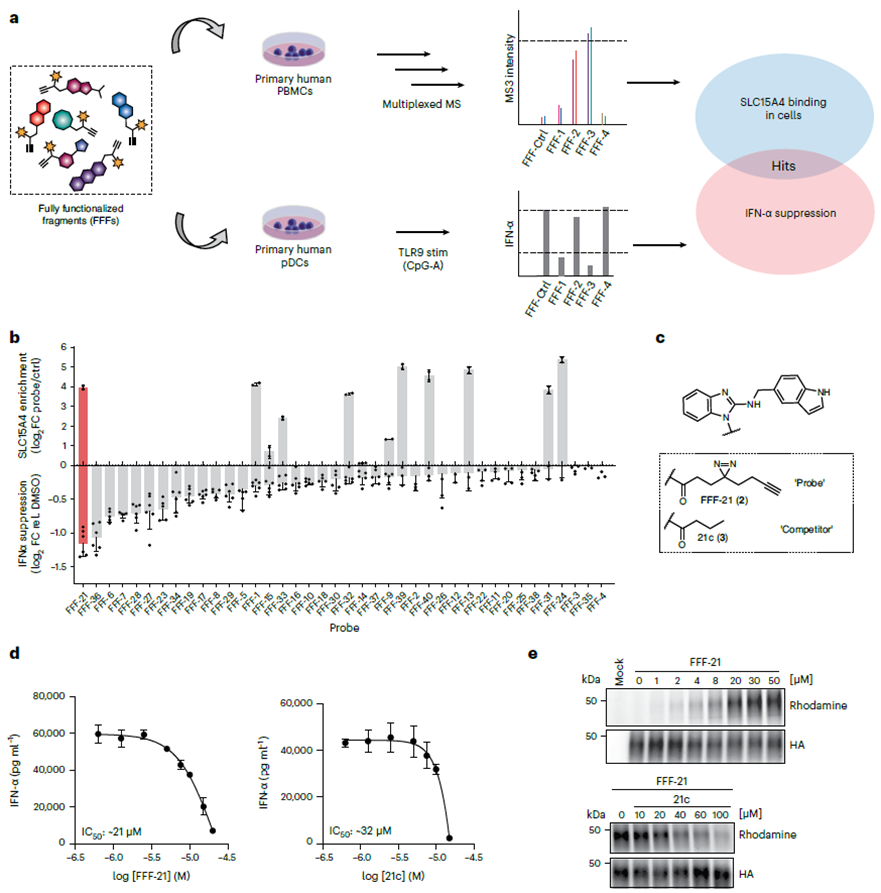
2. Modyfikacja fotosieciująca inhibitorów SLC15A4.
Po wstępnej selekcji związku FFF-21c autorzy przystąpili do optymalizacji jego struktury. Dzięki syntezie kilku analogów FFF-21c zidentyfikowali AJ 2-30 jako najsilniejszy inhibitor. Stosując techniki fotosieciowania, potwierdzili jego interakcję z celem. Następnie, wykorzystując zarówno metodę bezpośredniego znakowania, jak i metodę pośredniej konkurencji ABPP, wraz z komórkową analizą przesunięcia termicznego (CETSA), autorzy ostatecznie ustalili, że SLC15A4 jest głównym celem AJ 2-30.
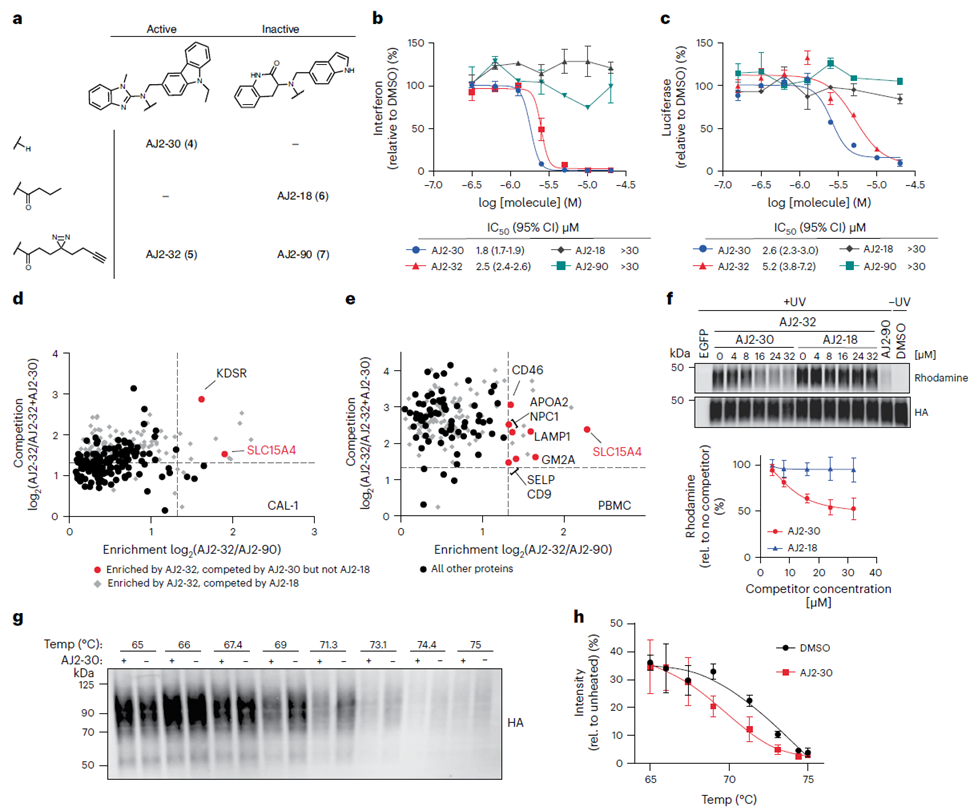
3. Mechanizm przeciwzapalny ujawnia, że AJ 2-30 zakłóca stabilność SLC15A4.
Po potwierdzeniu wiązania AJ 2-30 z SLC15A4 i jego działania hamującego, autorzy przeprowadzili serię eksperymentów biochemicznych w celu wyjaśnienia mechanizmu przeciwzapalnego AJ 2-30. Wyniki ujawniły, że AJ 2-30 indukuje degradację SLC15A4 za pośrednictwem lizosomów poprzez destabilizację białka, hamując w ten sposób aktywację TLR 7-9 i NOD w komórkach układu odpornościowego w sposób zależny od SLC15A4. To podkreśla potencjał AJ 2-30 w leczeniu chorób zapalnych i autoimmunologicznych.
Podsumowując, w tym badaniu umiejętnie wykorzystano techniki proteomiki chemicznej w celu zidentyfikowania AJ 2-30, silnego inhibitora SLC15A4 o niezwykłej aktywności przeciwzapalnej. Związek ten wykazuje znaczną skuteczność w modelach zwierzęcych poprzez specyficzne ukierunkowanie na stabilność SLC15A4 i jego rolę w prezentacji antygenu i szlakach sygnalizacji stanu zapalnego. Ten kluczowy postęp nie tylko pogłębia naszą wiedzę na temat przeciwzapalnych celów terapeutycznych, ale także kładzie solidne podstawy pod przyszły rozwój nowych środków terapeutycznych na różne choroby zapalne i autoimmunologiczne. Dzięki dalszym badaniom i walidacji klinicznej te nowe inhibitory SLC15A4 mogą zapewnić bardziej precyzyjne i skuteczne opcje leczenia wielu pacjentów, wywierając w ten sposób głęboki wpływ na zdrowie na całym świecie.

