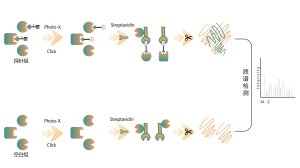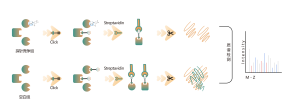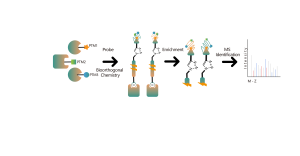Produkty
Chemoproteomiczne odkrycie nowych struktur wiodących dla celów niemożliwych do leczenia
Tło techniczne
Obecnie leki zatwierdzone przez FDA celują jedynie w około 800 białek, a duża liczba celów związanych z chorobami jest „nie do wyleczenia”. Ponieważ obecnie większość technologii opiera się na oczyszczonych białkach. Pojawienie się chemproteomiki zrewolucjonizowało odkrywanie leków – od oczyszczonych białek po żywe komórki. Jest w stanie ilościowo analizować oddziaływania pomiędzy małymi cząsteczkami i białkami w skali ludzkiego proteomu. Obecnie w lizatach komórkowych i żywych komórkach wykazano odkrycie struktur kowalencyjnych wobec specyficznych reszt aminokwasowych celów białkowych, takich jak cysteina, lizyna, metionina i tyrozyna. ChomiX wykorzysta własną platformę chemoproteomiki, aby szybko przełamać bariery celów „nie do pokonania”.

Zalety techniczne
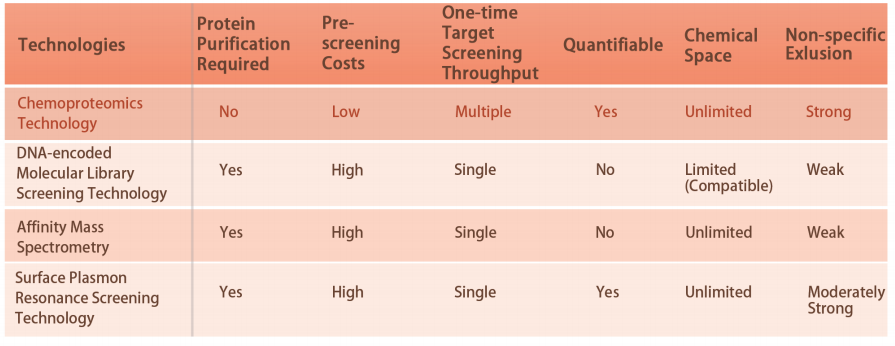
Funkcje techniczne platformy
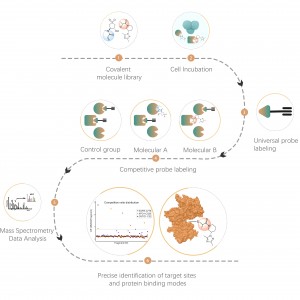
Platforma DIA-ABPP ma na celu odkrywanie kowalencyjnych środków wiążących, które angażują cele białkowe poprzez reakcje kowalencyjne z grupą tiolową reszt cysteiny. Gdy aktywne reszty cysteinowe białek zostaną preferencyjnie zajęte przez cząsteczki kowalencyjne, konkurowany będzie znacznik uniwersalnej sondy, który specyficznie reaguje z grupą tiolową. W połączeniu z ilościowymi technikami proteomiki opartymi na DIA, można określić ilościowo intensywność znakowanych sondą peptydów pomiędzy cząsteczką kowalencyjną a grupą kontrolną. Te różnice w sygnałach reprezentują stopień zajęcia cząsteczek kowalencyjnych w stosunku do ich białek wiążących. W przeciwieństwie do tradycyjnych strategii przeszukiwania pojedynczego celu, platforma DIA-ABPP umożliwia ilościową analizę interakcji pomiędzy fragmentami elektrofilowymi i prawie wszystkimi białkami w żywych komórkach z rozdzielczością reszt aminokwasowych, co znacznie poprawia wydajność i zmniejsza ryzyko w przypadku wysokowydajnego projektu odkrywania struktur wiodących .

Przebieg pracy podczas badania przesiewowego kowalencyjnych związków ołowiu
Cecha 1

Nasza biblioteka cząsteczek podobnych do leków zawiera różnorodne grupy reaktywne (głowice bojowe) charakteryzujące się łagodną reaktywnością elektrofilową, takie jak akrylamid, chloroacetamid i alkinoamid. Cząsteczki te charakteryzują się strukturalnie zróżnicowanymi farmakoforami zgodnymi z Zasadą Pięciu Lipińskiego.
Cecha 2

Obecnie biblioteka celów białkowych wychwytywanych przez sondę chemiczną specyficzną dla tiolu obejmuje 39962 miejsca cysteinowe z 12421 białek, w tym kinazy, fosfatazy, ligazy i czynniki transkrypcyjne. Biblioteka jest na bieżąco aktualizowana, zapewniając dostęp do najświeższych informacji na temat konkretnych celów i obiektów. Szczegółowe informacje dotyczące konkretnych celów i lokalizacji można znaleźć pod poniższym linkiem.
Cecha 3

W pojedynczym eksperymencie przesiewowym platforma jest w stanie określić ilościowo docelowe zaangażowanie małych cząsteczek (A2-H6) w stosunku do wszystkich znakowanych białek w całym proteomie. Powyższy rysunek przedstawia zajęcie miejsca wybranych klinicznie ważnych celów przez cząsteczki kowalencyjne. Im ciemniejszy kolor, tym większe zajęcie cząsteczek w kieszeniach wiążących, w tym w miejscach ortosterycznych i allosterycznych (gwiazdka wskazuje, że stopień obłożenia jest wyższy niż 80%). Zatem powinowactwo i selektywność każdej cząsteczki można ocenić jednocześnie w celu późniejszej optymalizacji struktury.