[Avanço de alta pontuação] Avanço na regulação antiinflamatória de SLC15A4 com o novo inibidor AJ 2-30: uma abordagem de proteômica química (IF 14.8)
Este artigo emprega proteômica química para desenvolver e rastrear uma série de novos inibidores direcionados ao SLC15A4, uma proteína transmembrana inflamatória crucial altamente expressa em células apresentadoras de antígenos. O direcionamento inicial de potenciais inibidores utilizou a estratégia de biblioteca de sondas de fragmentos totalmente funcionalizados (FFF), identificando o FFF-21 como um potente inibidor da produção de IFN-α entre numerosas sondas. A otimização estrutural subsequente levou ao desenvolvimento do composto AJ 2-30, que não apenas demonstrou excelente inibição, mas também confirmou o SLC15A4 como seu principal alvo de modificação pós-fotocruzamento. Investigações posteriores revelaram que o AJ 2-30 exerceu potentes efeitos anti-inflamatórios ao reduzir a estabilidade do SLC15A4, induzindo a sua degradação através da via lisossómica e inibindo eficazmente a activação de TLR 7-9 e NOD. Este estudo não só é pioneiro com sucesso nos inibidores SLC15A4 com atividade anti-inflamatória significativa, mas também abre caminho para o desenvolvimento de novos medicamentos anti-inflamatórios.

Rota de Pesquisa
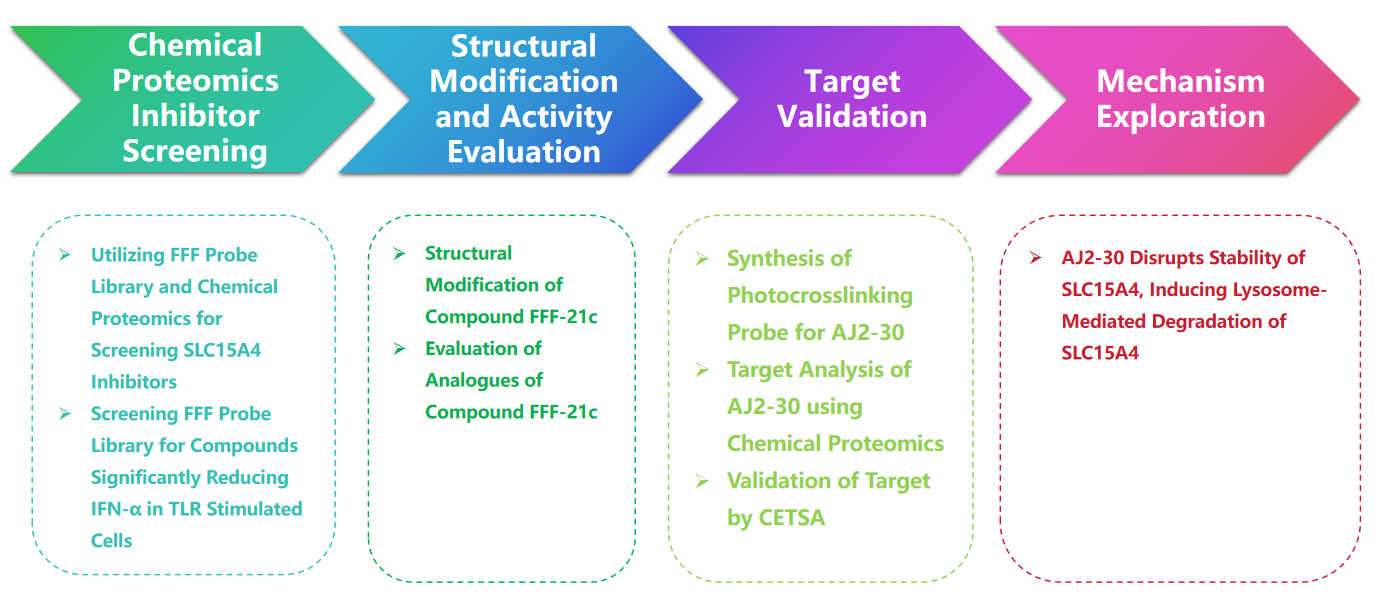
Processo experimental
1. Estratégia de biblioteca de sonda de fragmento totalmente funcionalizado (FFF) para rastrear inibidores de SLC15A4.
Os autores iniciaram seu estudo selecionando inibidores de SLC15A4 usando uma biblioteca de sondas de fragmentos totalmente funcionalizados (FFF). Este FFF compreende dois componentes: um grupo de reconhecimento molecular contendo fragmentos de comprimido projetados para atingir SLC15A4, e outro grupo enriquecido foto-reticulado apresentando grupos duplos de acrimidina e alcino para visualizar SLC15A4. Empregando um fluxo de trabalho proteômico químico, os autores confirmaram a ligação desta biblioteca de sondas FFF ao SLC15A4 nas células e avaliaram se a sonda FFF poderia atenuar os níveis de IFN-α em células estimuladas por TLR 9. Os resultados demonstraram que entre todas as sondas FFF que se ligam ao SLC15A4, o FFF-21 exibiu a maior capacidade de inibir os níveis de IFN-α, com o seu análogo sem marcador, FFF-21c, também apresentando efeitos inibitórios semelhantes.
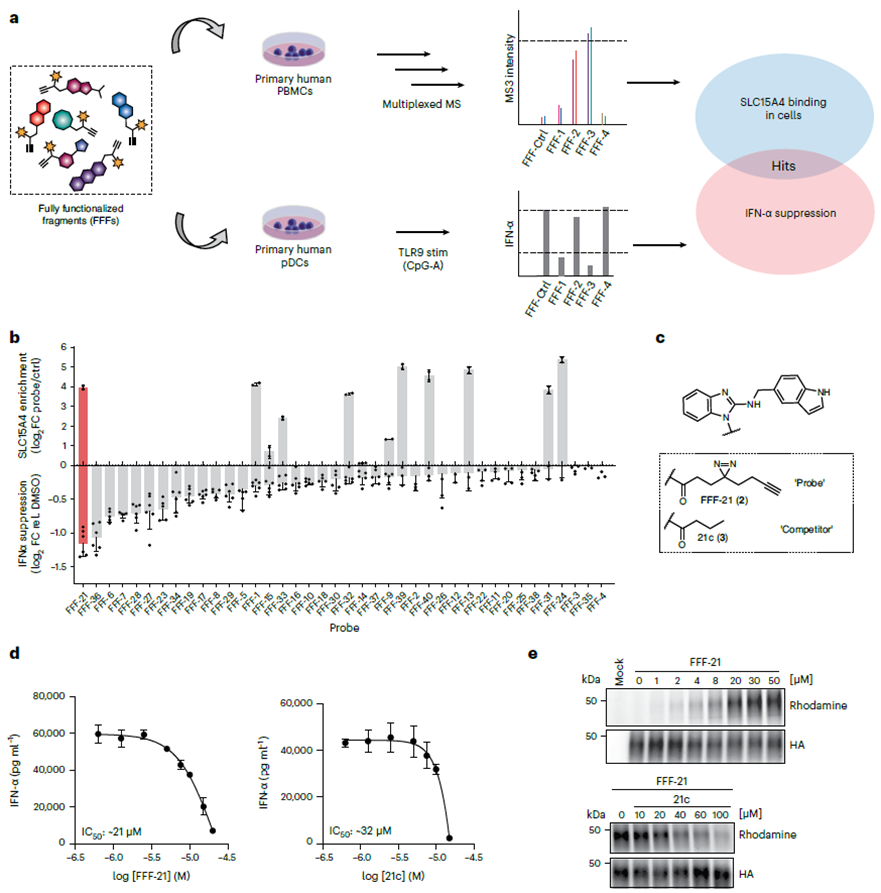
2. Modificação de fotocruzamento dos inibidores SLC15A4.
Após a seleção inicial do composto FFF-21c, os autores procederam à otimização da sua estrutura. Através da síntese de vários análogos do FFF-21c, identificaram o AJ 2-30 como o inibidor mais potente. Empregando técnicas de fotocruzamento, eles confirmaram sua interação com o alvo. Posteriormente, utilizando o método de marcação direta e o método de competição indireta da ABPP, juntamente com a análise de deslocamento térmico celular (CETSA), os autores estabeleceram definitivamente o SLC15A4 como o alvo principal do AJ 2-30.
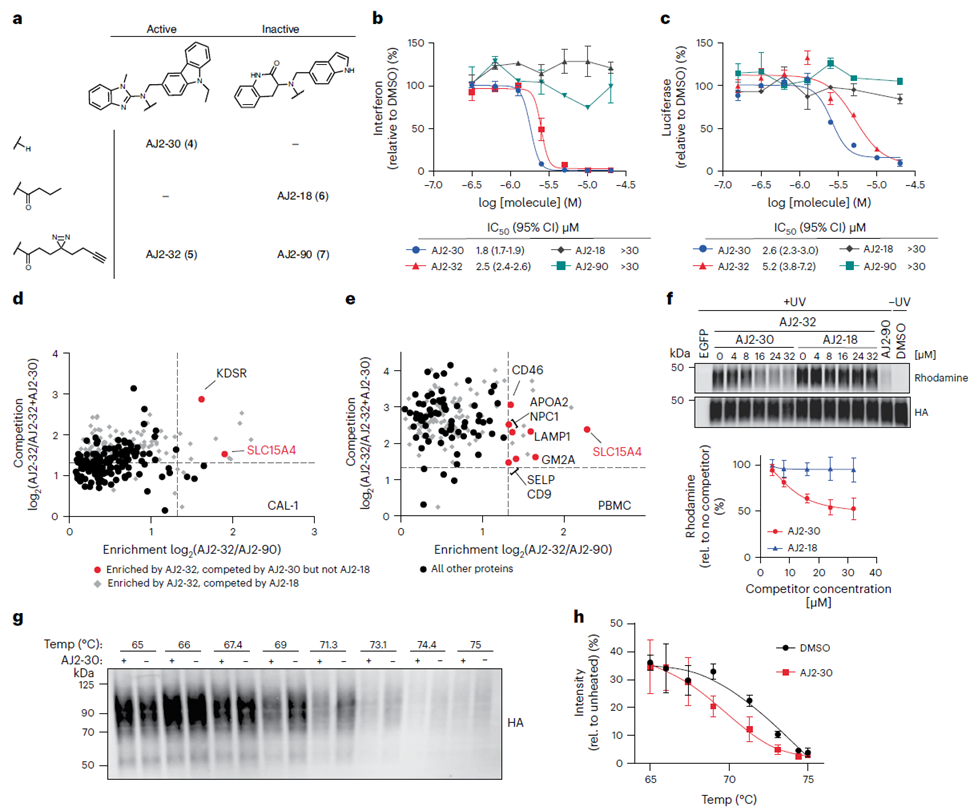
3. O mecanismo antiinflamatório revela que o AJ 2-30 perturba a estabilidade do SLC15A4.
Após a confirmação da ligação do AJ 2-30 ao SLC15A4 e do seu efeito inibitório, os autores conduziram uma série de experiências bioquímicas para elucidar o mecanismo anti-inflamatório do AJ 2-30. Os resultados revelaram que AJ 2-30 induz a degradação de SLC15A4 mediada por lisossoma, desestabilizando a proteína, inibindo assim a activação de TLR 7-9 e NOD em células imunitárias de um modo dependente de SLC15A4. Isto sublinha o potencial do AJ 2-30 no tratamento de doenças inflamatórias e autoimunes.
Em resumo, este estudo utiliza habilmente técnicas de proteômica química para identificar AJ 2-30, um potente inibidor de SLC15A4 com notável atividade antiinflamatória. Este composto demonstra eficácia significativa em modelos animais, visando especificamente a estabilidade do SLC15A4 e seu papel na apresentação de antígenos e nas vias de sinalização inflamatória. Este avanço fundamental não só melhora a nossa compreensão dos alvos terapêuticos anti-inflamatórios, mas também estabelece uma base robusta para o desenvolvimento futuro de novos agentes terapêuticos para uma variedade de doenças inflamatórias e autoimunes. Com mais pesquisas e validação clínica, estes novos inibidores SLC15A4 estão preparados para oferecer opções de tratamento mais precisas e eficazes para uma infinidade de pacientes, causando assim um impacto profundo na saúde global.

