
Produtos
Novas perspectivas terapêuticas para a medicina tradicional: a tecnologia ABPP revela o novo alvo antiinflamatório EIF2AK2 da Berberine
A medicina tradicional está sendo revitalizada com novas aplicações farmacológicas, à medida que técnicas avançadas, como o Perfil de Proteína Baseado em Atividade (ABPP), lançam luz sobre mecanismos terapêuticos até então desconhecidos. Neste contexto, a tecnologia da ABPP revelou recentemente um novo alvo anti-inflamatório da berberina, um composto extraído de plantas medicinais tradicionais chinesas e vulgarmente conhecido como Coptisina ou Huanglian na China. A descoberta destaca o EIF2AK2 como um interveniente fundamental nos efeitos anti-inflamatórios da berberina, abrindo novos caminhos para a sua utilização no tratamento de doenças relacionadas com a inflamação. Este avanço sublinha o potencial de reaproveitamento e otimização de medicamentos tradicionais através de métodos científicos modernos.

A berberina, um alcalóide tradicional com amplos efeitos farmacológicos, incluindo antiinflamatório, hipoglicemia e proteção cardiovascular, tem atraído atenção considerável. No entanto, os seus mecanismos moleculares precisos, particularmente na supressão da inflamação, permanecem obscuros.
Este estudo preenche esta lacuna de conhecimento utilizando a tecnologia ABPP para identificar o EIF2AK2 como um alvo crítico envolvido pela berberina pela sua ação anti-inflamatória. As descobertas aprofundam a nossa compreensão do mecanismo da berberina e fornecem uma base científica para o reposicionamento da berberina e o desenvolvimento de novos medicamentos anti-inflamatórios direcionados ao EIF2AK2.
A equipa empregou métodos quimioproteómicos avançados para investigar sistematicamente as interacções da berberina com proteínas intracelulares, confirmando a sua ligação específica ao EIF2AK2 e a modulação da sua actividade enzimática. Isto influencia as vias de resposta inflamatória, inibindo eficazmente a progressão da inflamação. Este avanço significativo oferece informações sobre o mecanismo anti-inflamatório da berberina e apoia o desenvolvimento de novas terapias direcionadas ao EIF2AK2.
A ChomiX fornece serviços de ponta como ABPP e CETSA para ajudar os pesquisadores na exploração de mecanismos de medicamentos e na aceleração dos esforços de desenvolvimento de novos medicamentos.
Rota de Pesquisa
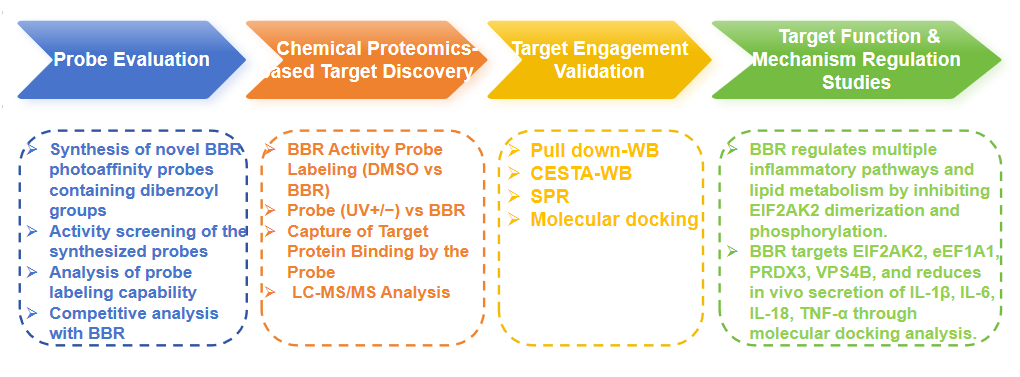
Processo experimental
1. A sonda 11b foi empregada como ferramenta funcional na pesquisa proteômica.
Os autores sintetizaram e rastrearam novas sondas de fotoafinidade BBR contendo grupos dibenzoíla em macrófagos THP-1 ativados por LPS + Nigericina. Entre estes, os compostos 7a e 11b apresentaram efeitos inibitórios dependentes do tempo e da dose na expressão de IL-1β, demonstrando eficácia aumentada em comparação com o composto original BBR. Através da análise do Perfil de Proteína Baseado em Atividade (ABPP) e da varredura de fluorescência, foi comprovado que tanto 7a quanto 11b se ligam efetivamente às suas proteínas alvo e exibem inibição competitiva, indicando assim um mecanismo de ação semelhante ao da BBR. Com base na observação de que o composto 11b exibiu alterações marcantes na intensidade de fluorescência dentro da faixa de concentração de 2,5% a 25%, particularmente em uma concentração de 20 milimolar onde a variação do sinal de fluorescência era mais proeminente, ele foi escolhido como sonda funcional para estudos proteômicos. . Esta seleção foi fundamentada em sua capacidade de resposta superior, o que a torna adequada para elucidar interações proteicas em um ambiente proteômico.
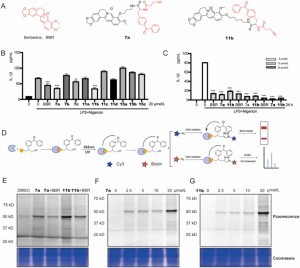
Figura 1: Triagem e avaliação de sondas BBR.
2. A nova sonda 11b identificou 44 proteínas alvo de BBR relacionadas à inflamação em células THP-1 e revelou EIF2AK2, eEF1A1, PRDX3 e VPS4B como alvos diretos com interações específicas com BBR.
Os autores, através de uma série de experimentos, empregaram com sucesso a nova sonda 11b para marcar e purificar potenciais proteínas alvo nas células THP-1. Em seguida, eles utilizaram a análise LC-MS/MS para identificar 44 proteínas associadas à inflamação na faixa de peso molecular de 20 a 80 kDa, entre as quais seis desempenharam papéis potencialmente críticos nas ações antiinflamatórias da BBR. Em investigações posteriores, EIF2AK2, eEF1A1, PRDX3 e VPS4B foram confirmados como alvos diretos da BBR, exibindo efeitos de inibição competitiva sob altas concentrações de tratamento com BBR. Esta descoberta revelou a provável existência de interações específicas entre estas proteínas e a BBR, elucidando assim novos conhecimentos sobre o seu envolvimento com o fármaco durante os seus processos anti-inflamatórios.
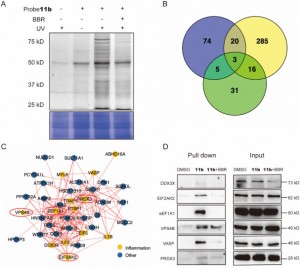
Figura 2: Captura de proteínas alvo e análise funcional.
3. A pesquisa em biologia estrutural elucida como a BBR modula a dimerização de EIF2AK2 para exercer seus efeitos antiinflamatórios por meio de interações de íons críticos e ligação cátion-pi.
Os autores empregaram técnicas CETSA, SPR e de acoplamento molecular para validar as interações entre BBR e quatro proteínas – EIF2AK2, eEF1A1, PRDX3 e VPS4B – em células HEK-293. Os resultados mostraram que a BBR aumentou a estabilidade térmica destas quatro proteínas, com a afinidade mais forte observada para EIF2AK2. Investigações adicionais revelaram que a ligação da BBR ao EIF2AK2 depende principalmente de pares de íons envolvendo D316 e E367 na cavidade II, bem como interações cátion-pi com K291. Este sítio de ligação está envolvido na dimerização de EIF2AK2, sugerindo que a BBR pode exercer seus efeitos antiinflamatórios modulando a dimerização de EIF2AK2.
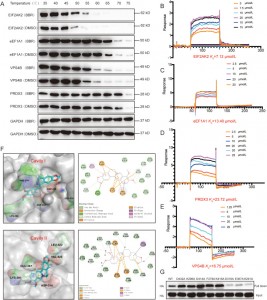
Figura 3: Estudos de afinidade entre a BBR e seus potenciais alvos.
4. O papel da BBR nas vias de inflamação e metabolismo lipídico é revelado, pois inibe a dimerização e fosforilação de EIF2AK2, demonstrando assim uma função fundamental na regulação do inflamassoma NLRP3, sinalização NF-kB p65/JNK/SIRT1.
Experimentos de imunoprecipitação confirmaram que a BBR inibe a dimerização de EIF2AK2, afetando tanto a autofosforilação de EIF2AK2 quanto a fosforilação de seu substrato eIF2a, revelando assim que a BBR regula o inflamassoma NLRP3, NF-kB p65, vias de sinalização JNK e expressão de SIRT1, desempenhando um papel crucial nas respostas inflamatórias celulares, mecanismos antiinflamatórios cerebrais (como na doença de Alzheimer) e induzidos por ácidos graxos estresse do retículo endoplasmático. Além disso, o silenciamento ou superexpressão de EIF2AK2 alterou significativamente os efeitos regulatórios da BBR em p-JNK e SIRT1, comprovando ainda que a BBR atua através da ligação a EIF2AK2 para regular distúrbios metabólicos lipídicos relacionados à inflamação.
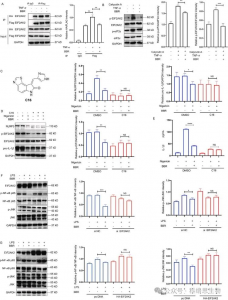
Figura 2 Captura de proteínas alvo e análise funcional.
5. Ao visar EIF2AK2, eEF1A1, PRDX3 e VPS4B, a BBR ajusta múltiplas vias inflamatórias, com EIF2AK2 desempenhando um papel regulador dominante entre estes alvos.
Para explorar ainda mais essa interação, os autores estabeleceram modelos de superexpressão e knockdown das quatro proteínas, demonstrando que a BBR modula seletivamente as vias inflamatórias JNK, NF-kB, MAPK e AKT, com EIF2AK2 desempenhando um papel dominante, o que foi validado em experimentos in vivo .
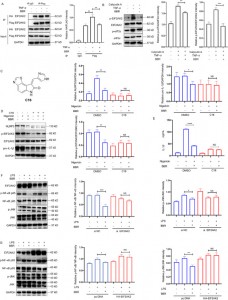
Figura 5: Estudos funcionais das proteínas alvo da BBR
6. Através do direcionamento específico de EIF2AK2, a BBR regula negativamente a secreção in vivo de IL-1β, IL-6, IL-18 e TNF-α; o knockdown do gene EIF2AK2 diminui sua eficácia antiinflamatória e ações protetoras do fígado.
Eles então investigaram se a BBR afeta a liberação de IL-1β, IL-6, IL-18 e TNF-α visando o EIF2AK2 in vivo. Para fazer isso, eles criaram um modelo de camundongo knockout para o gene EIF2AK2 usando injeção intravenosa de vírus adeno-associado (AAV) carregando shEIF2AK2. Camundongos knockout de tipo selvagem e EIF2AK2 receberam BBR (3 mg/kg) por via intraperitoneal seguido de injeção de LPS. Embora a BBR tenha reduzido significativamente os níveis de IL-1β, IL-6, IL-18 e TNF-α no grupo controle, esse efeito foi atenuado no grupo knockout para EIF2AK2. O exame histológico através da coloração H&E do tecido hepático indicou que o efeito melhorador da BBR na infiltração da inflamação hepática foi enfraquecido em camundongos knockout para EIF2AK2. Estas descobertas sugerem que a BBR potencialmente regula negativamente a secreção de IL-1β, IL-6, IL-18 e TNF-α através do direcionamento de EIF2AK2 e apresenta boa segurança.
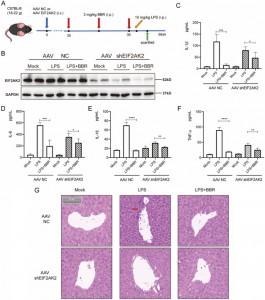
Figura 6: verificações funcionais EIF2AK2 in vivo.
Este estudo demonstra plenamente as poderosas vantagens da tecnologia ABPP na elucidação dos mecanismos complexos de moléculas bioativas como a berberina, impulsionando o avanço da pesquisa moderna em medicamentos tradicionais. Ao descobrir novos alvos e mecanismos de acção para a antiga droga berberina, não só enriquece a nossa compreensão das funções biológicas dos medicamentos tradicionais, mas também abre novas perspectivas e possibilidades para o tratamento de doenças relacionadas com a inflamação. Este resultado prenuncia que, com o apoio de técnicas científicas modernas como a ABPP, os medicamentos mais tradicionais serão reaproveitados através da identificação dos seus alvos e mecanismos específicos, fazendo contribuições significativas para os esforços de saúde humana.
Referência:https://doi.org/10.1016/j.apsb.2022.12.009.
