[Прорыв с высокими оценками] Улучшение противовоспалительной регуляции SLC15A4 с помощью нового ингибитора AJ 2-30: подход химической протеомики (IF 14.8)
В этой статье используется химическая протеомика для разработки и скрининга ряда новых ингибиторов, нацеленных на SLC15A4, важнейший воспалительный трансмембранный белок, высоко экспрессируемый в антигенпрезентирующих клетках. При первоначальном нацеливании на потенциальные ингибиторы использовалась стратегия библиотеки зондов полностью функционализированного фрагмента (FFF), идентифицирующая FFF-21 как мощный ингибитор продукции IFN-α среди многочисленных зондов. Последующая структурная оптимизация привела к разработке соединения AJ 2-30, которое не только продемонстрировало превосходное ингибирование, но также подтвердило, что SLC15A4 является его основной целевой модификацией после фотосшивки. Дальнейшие исследования показали, что AJ 2-30 оказывает мощное противовоспалительное действие, снижая стабильность SLC15A4, вызывая его деградацию по лизосомальному пути и эффективно ингибируя активацию TLR 7-9 и NOD. Это исследование не только успешно открывает ингибиторы SLC15A4 со значительной противовоспалительной активностью, но также открывает путь для разработки новых противовоспалительных препаратов.

Маршрут исследования
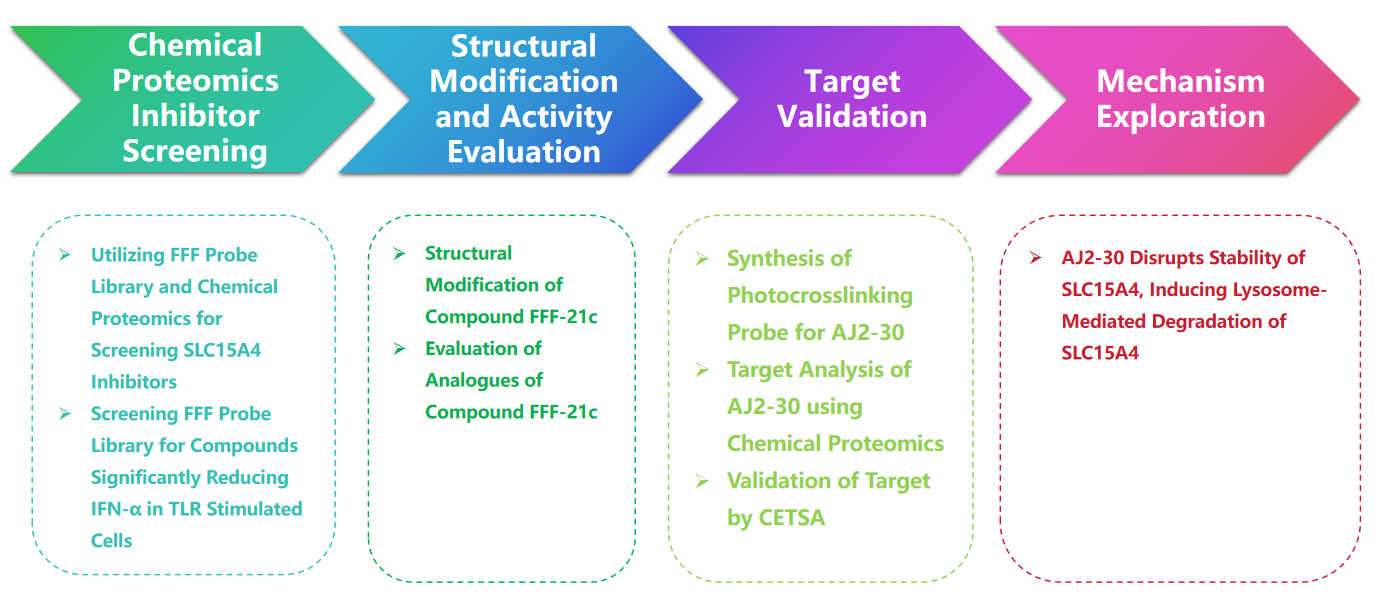
Экспериментальный процесс
1. Стратегия библиотеки зондов полнофункционализированного фрагмента (FFF) для скрининга ингибиторов SLC15A4.
Авторы начали свое исследование с скрининга ингибиторов SLC15A4 с использованием библиотеки зондов полностью функционализированного фрагмента (FFF). Этот FFF состоит из двух компонентов: одна группа молекулярного распознавания, содержащая фрагменты таблеток, предназначенные для нацеливания на SLC15A4, и другая обогащенная фотосшивкой группа, содержащая двойные акримидиновые и алкиновые группы для визуализации SLC15A4. Используя рабочий процесс химической протеомики, авторы подтвердили связывание этой библиотеки зондов FFF с SLC15A4 в клетках и оценили, может ли зонд FFF снижать уровни IFN-α в клетках, стимулированных TLR 9. Результаты показали, что среди всех зондов FFF, связывающихся с SLC15A4, FFF-21 продемонстрировал наибольшую способность ингибировать уровни IFN-α, а его немаркированный аналог FFF-21c также продемонстрировал аналогичные ингибирующие эффекты.
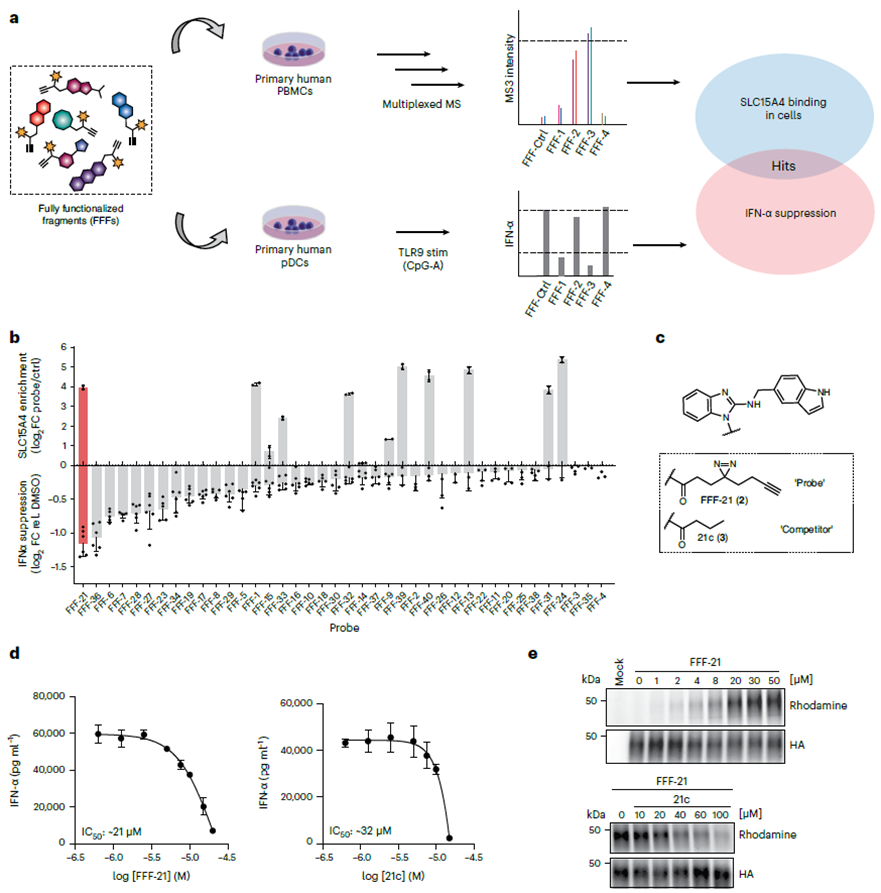
2. Фотосшивающая модификация ингибиторов SLC15A4.
После первоначального выбора соединения FFF-21c авторы приступили к оптимизации его структуры. Путем синтеза нескольких аналогов FFF-21c они определили AJ 2-30 как наиболее мощный ингибитор. Используя методы фотосшивки, они подтвердили его взаимодействие с мишенью. Впоследствии, используя как метод прямого мечения, так и метод непрямой конкуренции ABPP, а также анализ клеточного термического сдвига (CETSA), авт. окончательно установили SLC15A4 в качестве основной мишени AJ 2-30.
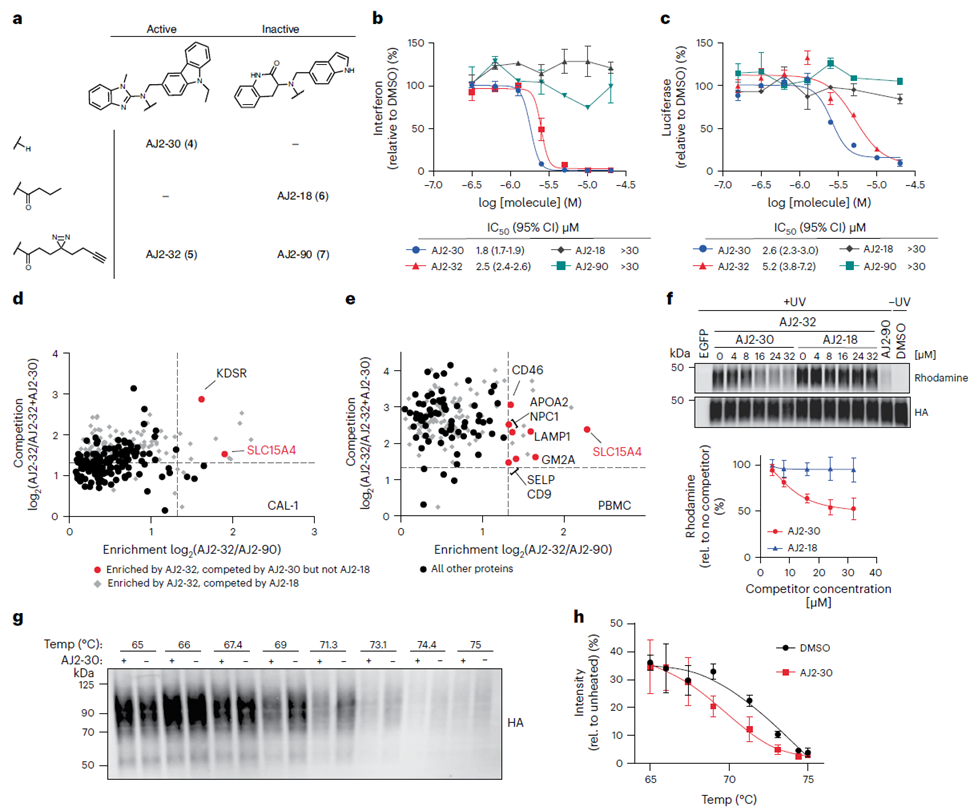
3. Противовоспалительный механизм показывает, что AJ 2-30 нарушает стабильность SLC15A4.
После подтверждения связывания AJ 2-30 с SLC15A4 и его ингибирующего эффекта авторы провели серию биохимических экспериментов, чтобы выяснить противовоспалительный механизм AJ 2-30. Результаты показали, что AJ 2-30 индуцирует опосредованную лизосомами деградацию SLC15A4 путем дестабилизации белка, тем самым ингибируя активацию TLR 7-9 и NOD в иммунных клетках SLC15A4-зависимым образом. Это подчеркивает потенциал AJ 2-30 в лечении воспалительных и аутоиммунных заболеваний.
Таким образом, в этом исследовании умело используются методы химической протеомики для идентификации AJ 2-30, мощного ингибитора SLC15A4 с замечательной противовоспалительной активностью. Это соединение демонстрирует значительную эффективность на животных моделях, специфически воздействуя на стабильность SLC15A4 и его роль в презентации антигена и воспалительных сигнальных путях. Это важнейшее достижение не только расширяет наше понимание целей противовоспалительной терапии, но и закладывает прочную основу для будущей разработки новых терапевтических средств для лечения различных воспалительных и аутоиммунных заболеваний. Благодаря дальнейшим исследованиям и клинической проверке эти новые ингибиторы SLC15A4 смогут предложить более точные и эффективные варианты лечения для множества пациентов, тем самым оказав глубокое влияние на глобальное здравоохранение.

