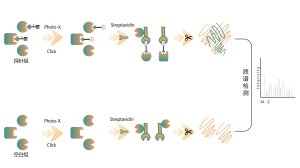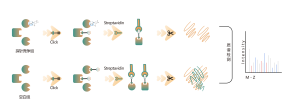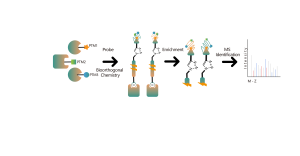Продукты
Идентификация нековалентных малых молекул лекарственных средств на основе фотоаффинных зондов
Техническая платформа
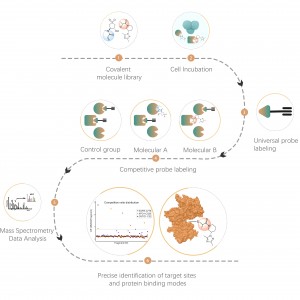
Платформа идентификации целей химической протеомики, основанная на фотоаффинных зондах, включает в себя несколько ключевых этапов, включая разработку зондов, синтез, оценку активности, маркировку, обогащение белками и анализ данных. Нековалентные низкомолекулярные лекарства, такие как синтетические соединения, экстракты трав, натуральные продукты и метаболиты, можно модифицировать в фотоаффинные зонды. Как только эти зонды связываются со своими мишенями внутри клеток, они образуют стабильные ковалентные взаимодействия, что позволяет избирательно обогащать и идентифицировать белки-мишени с низким содержанием.

Наши преимущества
1. Техническое совершенство: опытная команда, ведущие журнальные публикации и авторитетные отраслевые услуги.
2. Основная патентная технология: эксклюзивные патенты и передовое оборудование для поддержки ранней разработки лекарств.
3. Комплексное обслуживание: охватывает разработку зондов, синтез, обнаружение целей, биоинформатический анализ и своевременную обратную связь о ходе работы для удовлетворения потребностей клиентов.
4. Строгий контроль качества: сертификация ISO9001 гарантирует достоверность и достоверность отчетов.
Наш сервис
| Проект | Идентификация прямых мишеней для нековалентных низкомолекулярных лекарств |
| Образец | Рекомбинантный белок, клеточный лизат, живые клетки, больные ткани, кровь, бактерии, растительные ткани. |
| Аппаратная платформа | Бесконтактный ультразвуковой измельчитель клеток, система визуализации ChemiDoc MP, масс-спектрометр Orbitrap Fusion Lumos Tribrid/Orbitrap Exploris 480/Q Exactive HF-X/timsTOF Pro 2 |
| Продолжительность проекта | 4-8 недель |
| Результаты | Отчет о проекте (включая экспериментальные процедуры, диаграммы анализа данных, результаты биоинформатического анализа) |
Тематическое исследование
В ходе процесса скрининга лекарственных средств с использованием технологии скрининга жизнеспособности клеток было обнаружено, что соединение А оказывает значительное ингибирующее действие на клетки-мишени. Для дальнейшей идентификации целевых белков на молекулярном уровне, расшифровки механизма его действия и изучения потенциальных новых мишеней наша компания разработала и синтезировала фотореактивный зонд Probe A (включающий фотореактивные и биоортогональные группы) на основе структуры и характеристик активности соединения A. Используя технологическую платформу химической протеомики, мы применили методы флуоресцентного мечения и масс-спектрометрии для идентификации целевого белка в клеточных линиях, имеющих отношение к активности. В сочетании с методами биоинформатического анализа мы углубились в механизм действия соединения А и связанных с ним новых целевых белков.

На основании анализа флуоресцентного геля эксперимента по мечению, Зонд А эффективно метит белки, и сигнал мечения может в значительной степени конкурировать с соединением А. Это указывает на то, что Зонд А имеет такое же целевое покрытие, что и соединение А, что делает его подходящим инструментом химического зонда для последующее обнаружение цели.




График «Вулкан» иллюстрирует результаты эксперимента «Зонд А против ДМСО (Прямой)», в котором 114 белков (выделены красным на верхнем графике) были значительно обогащены зондом А. В эксперименте «Зонд А против (А+Зонд А)» (конкуренция) В эксперименте 38 белков (выделены красным на нижнем графике) были помечены зондом А и в значительной степени конкурировали с исходным соединением А. В этих двух экспериментах было получено 32 белка с высокой достоверностью связывания с соединением А. (n = 3, соотношение ≥ 2, значение p ≤ 0,05). Анализ GO Biological Pathway 32 белков с высокой достоверностью связывания с соединением A выявил значительное обогащение сигнальных путей, таких как отток фосфолипидов, негативная регуляция активности липазы и регуляция транспорта стеринов, что соответствует фенотипу.