利用化學蛋白質體學鑑定巨大戟二萜醇甲丁酸酯治療光化性角化症的功能性標靶 SLC25A20
這項研究利用化學蛋白質體學揭示了大分子丁酸甲酯 (Ing-Meb) 的新靶點,這是一種用於治療日光性角化症的藥物。研究團隊最初設計並合成了一種名為Ing-Dayne的Ing-Meb光親和探針,它在紫外光照射下與目標蛋白形成共價鍵,有助於識別潛在的功能標靶。透過隨後的驗證,作者確定 SLC25A20 是 Ing-Meb 的關鍵標靶。 SLC25A20 是一種參與脂肪酸代謝的粒線體膜結合肉鹼-醯基肉鹼轉位酶。值得注意的是,Ing-Meb 對 SLC25A20 功能的抑製作用導致長鏈醯基肉鹼的累積增加,證實 Ing-Meb 透過調節脂肪酸氧化途徑來發揮其治療作用。此外,該研究也深入探討了結構修飾在天然產物研究中的重要性。透過對Ing-Meb進行結構修飾合成Ing-Dayne光親和探針,研究人員成功發現了一個不同於常規理解的新標靶。這不僅增強了對 Ing-Meb 及其作用模式的理解,而且強調了結構修飾在化學蛋白質體學研究中對於揭示天然產物複雜性的關鍵作用。這些見解進一步推動藥物創新,包括優化現有藥物療效、開發針對特定實體的新療法以及闡明藥物副作用機制。
研究路線
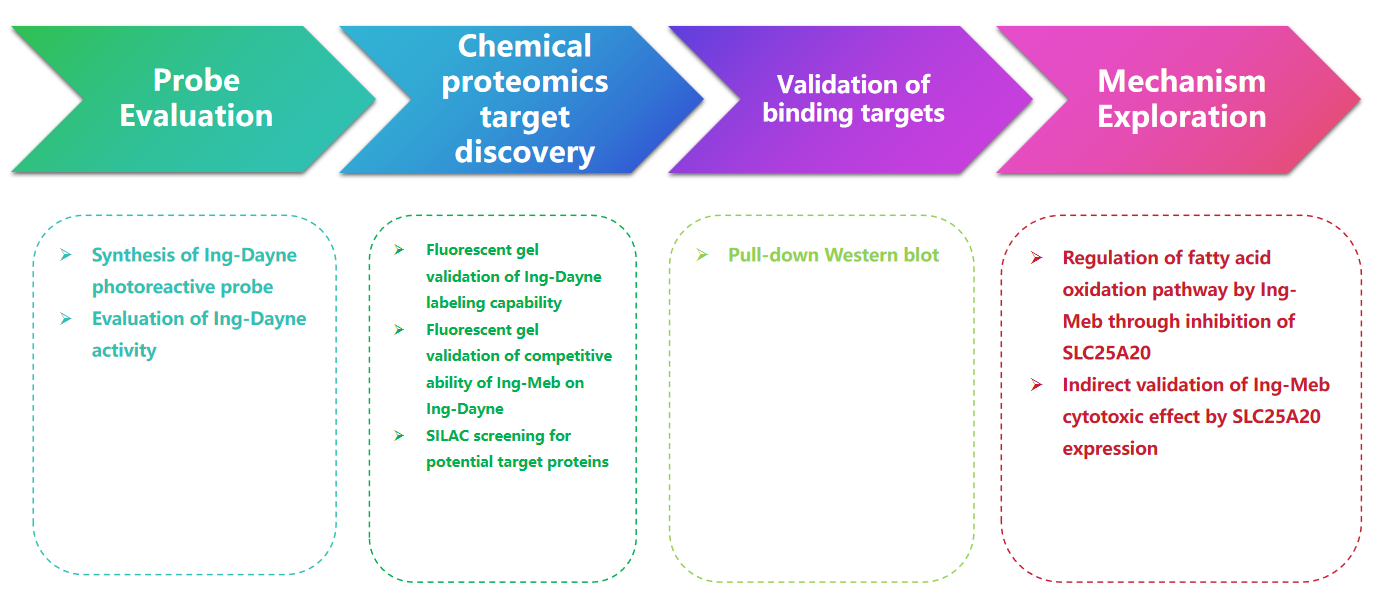
實驗過程
1. 設計合成的 Ing-Dayne 光親和探針揭示了光化性角化病藥物 Ing-Meb 與其標靶蛋白結合的機制。
在本研究中,使用了源自光化性角化症治療藥物 Ing-Meb 的 Ing 親和探針 Ing-Dayne(參見圖 1)。透過將此探針分子與特定細胞共培養並隨後進行紫外光照射,探針內的雙吖啶結構與細胞內蛋白質形成穩定的共價鍵。細胞裂解後,點選化學反應促進報告基團疊氮化物-四甲基羅丹明附著到目標蛋白上(如圖 2 所示)。隨後的 SDS-PAGE 分析(如圖 3 所示)顯示,Ing-Meb 對探針表現出顯著的競爭性結合效應,而 Ingenol 具有相似的結構,沒有表現出競爭性抑制。
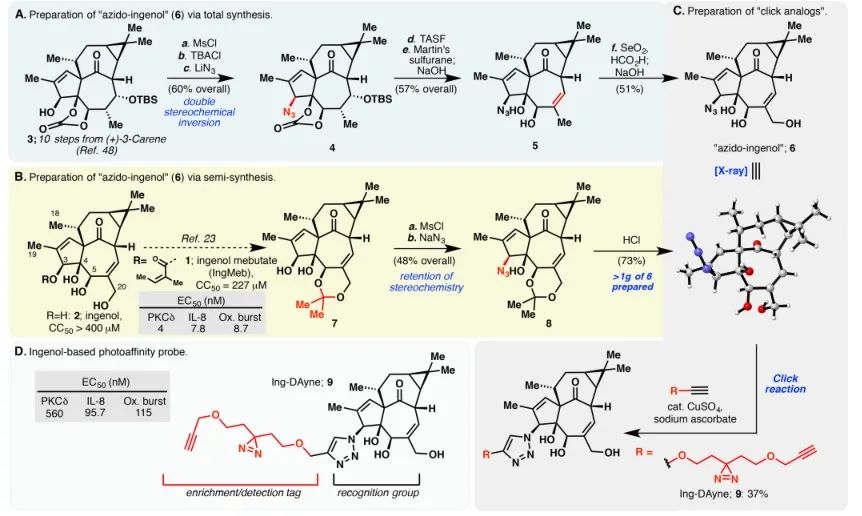
圖 1:說明了 Ing-Dayne 合成所採用的兩種合成路線。
2.新型探針11b鑑定了THP-1細胞內BBR的44個發炎相關標靶蛋白,並揭示了EIF2AK2、eEF1A1、PRDX3和VPS4B是與BBR具有特異性相互作用的直接靶點。
作者透過一系列實驗,成功地利用新型探針11b來標記和純化THP-1細胞內的潛在標靶蛋白。隨後,他們利用 LC-MS/MS 分析鑑定了 44 種分子量範圍為 20 至 80 kDa 的發炎相關蛋白,其中 6 種被發現可能在 BBR 的抗發炎作用中發揮關鍵作用。進一步研究中,EIF2AK2、eEF1A1、PRDX3和VPS4B被證實是BBR的直接標靶,在高濃度BBR處理下表現出競爭性抑製作用。這項發現揭示了這些蛋白質和 BBR 之間可能存在的特定相互作用,從而闡明了它們在抗發炎過程中與藥物相互作用的新見解。
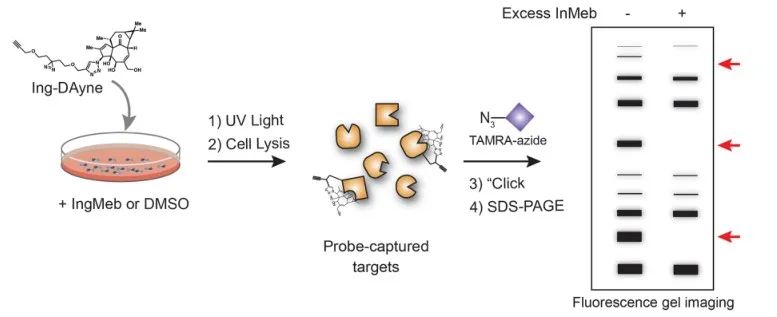
圖 2:Ing-Dayne 標靶基於凝膠的驗證過程。
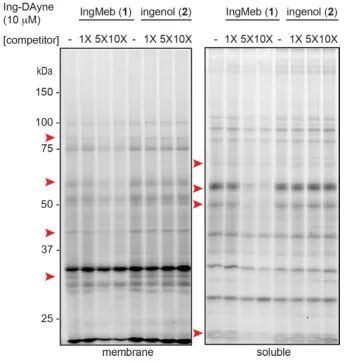
圖 3:Ing-Meb 和巨大戟二萜醇對探針分子 Ing-Dayne 的競爭性抑制。
3. SILAC篩選結合Western blot驗證,確定SLC25A20為Ingenol類藥物Ing-Meb的主要標靶。
作者最初使用細胞培養胺基酸穩定同位素標記 (SILAC) 技術篩選了 28 種潛在標靶蛋白(圖 4)。隨後,透過進一步的篩選和Western blot驗證實驗(圖5),研究人員觀察到,在這些候選靶點中,Ing-Meb對SLC25A20表現出最強的抑製作用,強烈表明SLC25A20是Ing-Meb的核心功能靶點之一。
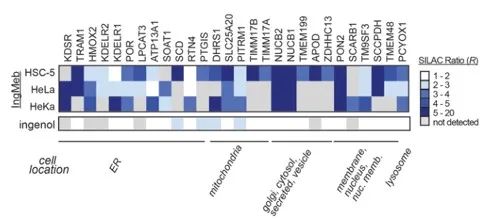
圖4:初步篩選得到的28個潛在標靶。
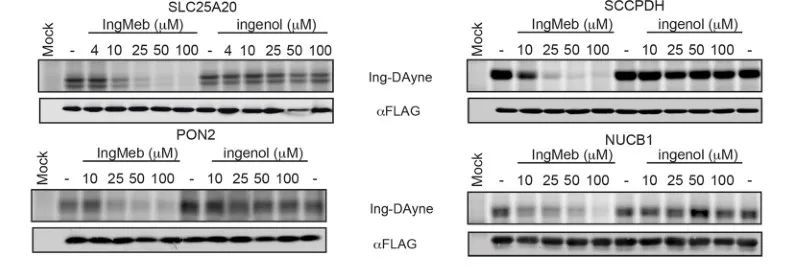
圖 5:四種潛在標靶蛋白的蛋白質印跡實驗。
4. Ing-Meb 透過抑制 SLC25A20(一種粒線體膜蛋白,也稱為肉毒桿菌鹼脂醯轉移酶)來調節脂肪酸氧化途徑,從而揭示其作為光化性角化病藥物的標靶。
作者研究了 SLC25A20,也稱為肉毒鹼硫辛酸轉移酶或 CACT,是一種位於粒線體膜內的多模式整合膜蛋白。其主要功能涉及將長鏈醯基肉鹼轉運至粒線體,促進其與遊離肉鹼的交換。這些轉運的醯基肉鹼隨後被肉鹼棕櫚醯轉移酶-2 (CPT-2) 轉化為脂肪醯基輔酶 A,從而作為脂肪酸 β-氧化的前驅物。實驗結果表明,隨著光化性角化病藥物 Ing-Meb 濃度的增加,細胞長鏈醯基肉鹼含量顯著增加(如圖 6 所示)。這項觀察結果有力地支持了Ing-Meb對SLC25A20的抑製作用,從而證實SLC25A20是介導Ing-Meb作用的主要標靶之一。
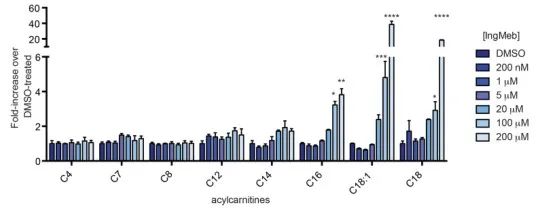
圖 6:Ing-Meb 對長鏈醯基肉鹼的影響
5.透過SLC25A20表達間接驗證Ing-Meb細胞毒性作用:揭示其在藥物活性調節中的目標功能。
研究人員試圖將 HeLa 細胞中 SLC25A20 的抑制與 Ing-Meb 的潛在細胞毒性作用直接聯繫起來。結果表明,雖然SLC25A20 的過度表現並未改變這些細胞中Ing-Meb 的半數抑制濃度,但值得注意的是,SLC25A20 表達的增加顯著減輕了Ing-Meb 對長鏈酰基肉鹼積累的影響(如圖7 所示) 。這項結果進一步證實了 SLC25A20 作為 Ing-Meb 藥物活性的關鍵功能標靶的假設。
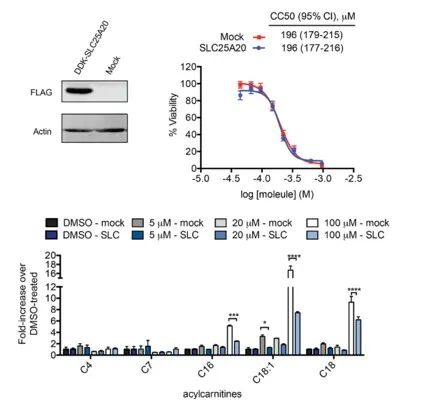
圖7:SLC25A20表現與否對CC50和醯基肉鹼的影響。
該研究不僅揭示了Ing-Meb的新靶點,也為結構複雜天然產物的標靶發現提供了新的理論基礎和策略方向。參考:

